题目内容
10.下列实验所对应的方案正确的是( )| 选项 | 目的 | 方案 |
| A | 除去木炭粉中的氧化铜 | 在空气中充分燃烧 |
| B | 分离NaCl和CaCO3的混合物 | 加足量稀盐酸,蒸发 |
| C | 区分稀盐酸和稀氢氧化钠溶液 | 分别测溶液的pH |
| D | 鉴别化肥NH4Cl和NH4NO3 | 取样,加熟石灰研磨 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据碳和氧气反应会生成二氧化碳进行解答;
B、根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,产物CaCl2无法分离进行解答;
C、根据盐酸显酸性,pH值小于7,氢氧化钠溶液,显碱性pH值大于7进行解答;
D、根据铵态氮肥和碱混合会生成氨气进行解答.
解答 解:A、消耗了主要物质木炭,所以不能用在空气中充分燃烧的方法除去木炭粉中的氧化铜,故A错误;
B、加入足量稀盐酸后,产物CaCl2无法与氯化钠分离,故B错误;
C、盐酸显酸性,pH值小于7,氢氧化钠溶液,显碱性pH值大于7,所以可用分别测溶液的pH的方法检验稀盐酸和稀氢氧化钠溶液,故C正确;
D、取样品,加熟石灰研磨都会生成氨气,故D错误.
故选:C.
点评 本题难度不大,但综合性较强,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
20.下列常见的材料中.属于合成材料的是( )
| A. | 玻璃 | B. | 钢筋混凝土 | C. | 陶瓷 | D. | 聚乙烯塑料 |
1.小明同学对超市一种新产品-“污渍爆炸盐”产生浓厚兴趣,该产品的主要成分是过氧碳酸钠(Na2CO4)在实验室,小明将污渍爆炸盐放入热水中,发现立即产生大量气泡,能使带火星的木条复燃.小明进一步将等浓度的过氧化氢溶液放入相同温度的热水中,发现此时的过氧化氢分解速率明显小于污渍爆炸盐的分解速率.
【提出问题】促进过氧化氢分解的微粒是什么?
【查阅资料】
1.过氧碳酸钠(Na2CO4)与水反应生成碳酸盐和过氧化氢;
2.可溶性盐在水溶液中都是以金属离子(或NH4+)和酸根离子的形式存在;
【作出猜想】猜想一:促进过氧化氢分解的微粒可能是水分子
猜想二:促进过氧化氢分解的微粒可能是Na+
猜想三:促进过氧化氢分解的微粒可能是CO32-
小松同学指出,不可能是水分子促进了过氧化氢的分解.你赞成(填“赞成”或“不赞成”),你的理由是过氧化氢溶液中就存在水分子,没有加快反应速率.
【设计实验】
【交流讨论】小松同学提出,上述实验方案不严谨,还需补充一个实验,请你帮他写出实验方案验证反应前后碳酸钠的化学性质和质量是否发生改变.
【提出问题】促进过氧化氢分解的微粒是什么?
【查阅资料】
1.过氧碳酸钠(Na2CO4)与水反应生成碳酸盐和过氧化氢;
2.可溶性盐在水溶液中都是以金属离子(或NH4+)和酸根离子的形式存在;
【作出猜想】猜想一:促进过氧化氢分解的微粒可能是水分子
猜想二:促进过氧化氢分解的微粒可能是Na+
猜想三:促进过氧化氢分解的微粒可能是CO32-
小松同学指出,不可能是水分子促进了过氧化氢的分解.你赞成(填“赞成”或“不赞成”),你的理由是过氧化氢溶液中就存在水分子,没有加快反应速率.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 向6%3mL的过氧化氢溶液中加入1mL 10%的NaCl溶液,深入一根带火星的木条 | 促进过氧化氢分解的微粒不是Na+ | 猜想二不成立 |
| 实验二 | 向 6%3mL的过氧化氢溶液中,加入1mL10%的K2CO3溶液,伸入一根带火星的木条 | 促进过氧化氢分解的微粒是CO32- | 猜想三成立 |
5.下列实验现象不正确的是( )
| A. | 打开浓盐酸的试剂瓶盖,瓶口会出现白雾 | |
| B. | 普通火柴头燃烧产生的气体能使高锰酸钾溶液褪色 | |
| C. | 向鸡蛋清溶液中加饱和硫酸铵溶液有沉淀析出 | |
| D. | 水通电时正极产生的气体燃烧发出淡蓝色火焰 |
2.硝酸盐分解很有规律.例如硫酸铜热分解可得氧化铜、四体积二氧化氮和一体积氧气,把硝酸铜热分解后产生的气体收集在一个大试管中,用带火星的木条检验,可以观察到的现象是( )
| A. | 带火星的木条复燃 | |
| B. | 带火星的木条与在空气中时现象一样 | |
| C. | 带火星的木条马上熄灭 | |
| D. | 无法判断 |
15.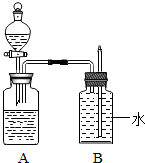 牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
 牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )| A. | 食盐和水 | B. | 硝酸铵和水 | C. | 镁和稀盐酸 | D. | 铜和稀硫酸 |