题目内容
5.金属在生产、生活中有着广泛的用途.(1)指出金属铁的一个性质及其对应的用途:性质导热性,对应用途铁锅.
(2)黄铜是铜锌合金,其硬度比纯铜大 (填“大”、“小”或“相同”).
(3)多数金属在自然界以矿物的形式存在,请写出一种含铁元素的矿石名称赤铁矿,用化学方程式表示工业炼铁的原理Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)长期露置于空气中的金属M表面会被锈蚀.经检测,锈蚀物中除含有M外,还含有碳、氢、氧三种元素.根据质量守恒定律,推测与金属M发生反应生成锈蚀物的物质.
推测Ⅰ:锈蚀物中的氢来自空气中的H2O(填化学式,下同),碳来自空气中的CO2,因此这两种物质肯定参加了反应.
推测Ⅱ:锈蚀物中的氧有多种来源,因此不能确定空气中的氧气是否参加了反应.
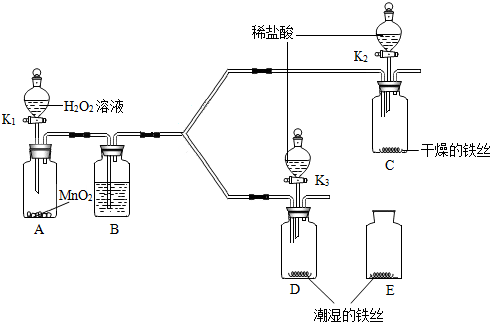
(4)某同学为了验证空气中的O2是否参加了反应,设计了如图所示的系列实验,你认为其中必须要做的实验是AF (填实验编号).
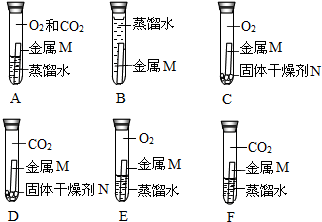
(说明:①所用蒸馏水都是经煮沸迅速冷却的;②固体干燥剂N只吸收水分,不吸收CO2和O2.)
分析 (1)根据金属的性质和用途分析;
(2)根据合金的性质分析;
(3)根据工业炼铁原理分析;
(4)根据金属锈蚀的条件和质量守恒定律分析解答;
(5)根据金属M锈蚀需要同时与水、氧气、二氧化碳接触,分析所设计的一组实验中可以通过是否锈蚀判断出与氧气有关的实验;
解答 解:(1)铁具有导热性,可制成炊具;
(2)由于合金的硬度大于其组分中的金属,因此,由铜锌组成的黄铜合金的硬度大于纯铜的硬度;
(3)赤铁矿中的氧化铁能和一氧化碳反应生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(4)根据化学变化前后元素种类不变,反应生成锈蚀物中的氢元素应来自于空气中含氢元素的水、碳元素来自于空气中含碳元素的二氧化碳气体;
(5)实验A中金属M与水、氧气、二氧化碳同时接触而出现锈蚀,实验B中金属M只与水接触没有锈蚀,实验C中金属M只与氧气接触没有锈蚀,实验D中金属M只与二氧化碳接触没有锈蚀,实验E中金属M仅与氧气和水接触没有锈蚀,实验F中金属M仅与水和二氧化碳接触没有锈蚀;因此通过实验A中出现锈蚀与实验F中没有锈蚀的对比,可得到金属M锈蚀需要氧气的.
故答案为:(1)导热性;铁锅;
(2)大;
(3)赤铁矿(褐铁矿、黄铁矿、磁铁矿);Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(4)H2O;CO2;
(5)AF
点评 本题以探究金属M的锈蚀过程为平台,考查了合金的特性、利用质量守恒定律分析实验现象、评价实

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
15.下列物质属于纯净物的是( )
| A. | 铝合金 | B. | 大理石 | C. | 蒸馏水 | D. | 食醋 |
13.丁二酮(C4H6O2)可用作糖果增香剂.下列关于丁二酮的说法中正确的是( )
| A. | 丁二酮属于有机高分子化合物 | |
| B. | 丁二酮中含有氧分子 | |
| C. | 丁二酮中氧元素的质量分数最大 | |
| D. | 丁二酮中C、H、O元素的质量比为24:3:16 |
20.下列常见的材料中.属于合成材料的是( )
| A. | 玻璃 | B. | 钢筋混凝土 | C. | 陶瓷 | D. | 聚乙烯塑料 |
10.合理使用化肥能提高农作物的产量,化肥的种类有很多,下列化肥中属于复合肥的是( )
| A. | KCl | B. | CO(NH2)2 | C. | NH4HCO3 | D. | KNO3 |
14.清凉油具有散热、醒脑、提神的功效,其主要成分为薄荷脑(化学式为C10H20O),下列有关薄荷脑的说法错误的是( )
| A. | 薄荷脑是3种元素组成的有机物 | |
| B. | 1个薄荷脑分子中含有31个原子 | |
| C. | 薄荷脑中碳元素的质量分数大于氢元素的质量分数 | |
| D. | 薄荷脑中碳、氢元素的质量比为1:2 |