题目内容
20. 当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.
当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.(1)该物质含有3种元素;
(2)该物质中碳元素和氢元素的质量比是9:1;
(3)对苯二胺的化学式量(或相对分子质量)为108;
(4)对苯二胺中氢元素的质量分数为7.4%.(结果保留到0.1%).
分析 (1)根据对苯二胺化学式的含义进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)对苯二胺是由碳、氢、氮三种元素组成的.
(2)该物质中碳元素和氢元素的质量比是(12×6):(1×5)=9:1.
(3)对苯二胺的相对分子质量为12×6+1×8+14×2=108.
(4)对苯二胺中氢元素的质量分数为$\frac{1×5}{108}×$100%≈7.4%.
故答案为:(1)3;(2)9:1;(3)108;(4)7.4%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
8.小东从海边捡来一些嵌有砂砾的贝壳(主要成分是CaCO3),为测定碳酸钙的含量,他做了如下实验:首先称取50g贝壳样品,然后将150mL的盐酸分5次加入(假设其余杂质均不与盐酸反应),实验过程中的数据记录如下:
(1)X=30g;
(2)小东测得贝壳样品中碳酸钙的质量分数是90%;
(3)若把二氧化碳收集起来,共有19.8g.
| 稀盐酸的体积 | 第一次 30mL | 第二次 30mL | 第三次 30mL | 第四次 30mL | 第五次 30mL |
| 剩余固体质量 | 40.0g | X | 20.0g | 10.0g | 5.0g |
(2)小东测得贝壳样品中碳酸钙的质量分数是90%;
(3)若把二氧化碳收集起来,共有19.8g.
15.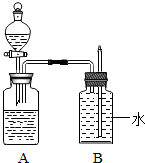 牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
 牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
牛牛同学设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )| A. | 食盐和水 | B. | 硝酸铵和水 | C. | 镁和稀盐酸 | D. | 铜和稀硫酸 |
5.某化工厂为综合利用生产过程中的副产品CaSO4,与相邻化肥厂联合设计了制备(NH4)2SO4的工艺流程(如图所示).在该流程中,沉淀池中发生的主要化学反应为:
CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
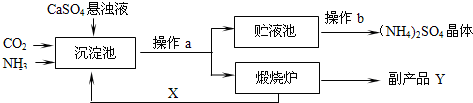
下列说法正确的是( )
CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4

下列说法正确的是( )
| A. | 该工艺中副产品Y为硫酸钙 | |
| B. | 操作b的过程是蒸发、冷却、结晶 | |
| C. | 该工艺中可循环使用的X为二氧化碳 | |
| D. | 实验室中进行操作a时,用到的玻璃仪器除玻璃棒、烧杯外,还需酒精灯 |
12.下列关于燃烧现象的描述中正确的是( )
| A. | 木炭在空气中燃烧后,生成黑色的固体 | |
| B. | 硫粉在氧气中燃烧,产生大量白烟 | |
| C. | 铁丝在空气剧烈燃烧火星四射 | |
| D. | 红磷在空气中燃烧,产生大量白烟 |
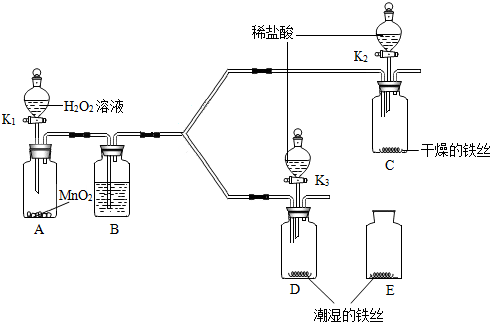

 明明同学在实验考试时,抽到的题目是“配制100g质量分数为6.5%的氯化钠溶液.”
明明同学在实验考试时,抽到的题目是“配制100g质量分数为6.5%的氯化钠溶液.”