题目内容
13.某科学兴趣小组对“煤炭是否含硫”这一问题产生了争论,他们设计了如图所示实验进行测定.
(1)他们查阅资料后找到了这样一段话:“二氧化硫能使KMnO4溶液褪色(由紫红色变成无色),反应方程式为:5SO2+2KMnO4+2H 2O═K2SO4+2MnSO4+2X”.
然而方程式中最后一种物质(X)的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测X的化学式为H2SO4.反应后生成的MnSO4中Mn元素化合价为+2.
(2)盐往往是由离子构成的.如:KMnO4由K+和MnO4-构成,K2SO4由K+和SO42-构成.盐的晶体或溶液的颜色通常是由构成它的离子决定的.请根据(1)中查阅到的资料推测:KMnO4溶液呈现的紫红色可能是由MnO4-离子表现出来的(填离子符号),理由是:反应后无色溶液中存在K+,说明K+无色,所以紫红色是由MnO4-表现出来的.
分析 (1)根据质量守恒定律,以及化合物中化合价的代数和为零进行分析;
(2)根据(2)中的信息,二氧化硫和高锰酸钾反应生成硫酸、硫酸钾、硫酸锰,三者的混合溶液呈无色,说明硫酸根离子、氢离子、锰离子均无色进行分析.
解答 解:(1)根据质量守恒定律,化学反应前后元素的种类和数目不变,反应物中有5个硫原子,20个氧原子,2个钾原子,2个锰原子,4和氢原子,生成物中有2个钾原子,3个硫原子,12个氧原子,2个锰原子,所以X的化学式为:H2SO4,在化合物中元素化合价的代数和为零,MnSO4中锰元素的化合价=0-(+6)-(-2)×4=+2;(2)二氧化硫和高锰酸钾反应生成硫酸、硫酸钾、硫酸锰,根据“二氧化硫能使KMnO4溶液褪色(由紫红色变成无色),反应后无色溶液中存在K+,说明K+无色,所以紫红色是由MnO4-表现出来的.
故答案为:(1)H2SO4,+2;
(2)MnO4-,反应后无色溶液中存在K+,说明K+无色,所以紫红色是由MnO4-表现出来的.
点评 综合实验涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
1.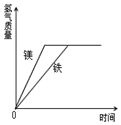 有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
下列结果可能的是( )
 有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.下列结果可能的是( )
| ①反应后镁有剩余 | ②反应后铁有剩余 |
| ③反应后稀硫酸有剩余 | ④反应后稀盐酸有剩余 |
| ⑤剩余铁的和镁的质量相等 | ⑥消耗的稀硫酸和稀盐酸质量相等. |
| A. | ①③⑤ | B. | ①②⑥ | C. | ①④ | D. | ②③⑥ |
8.现有甲、乙、丙三种金属,分别与空气和氧气反应,现象如表所示:
据以上信息,这三种金属活动性由强到弱的顺序是甲、丙、乙.
| 甲 | 乙 | 丙 | |
| 空气 | 剧烈燃烧 | 变黑 | 变黑 |
| 氧气 | 更剧烈燃烧 | 变黑 | 剧烈燃烧 |
5.某品牌矿泉水的标签上的内容如表所示,下列说法中,不正确的是( )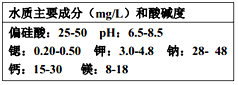

| A. | 该品牌矿泉水为混合物 | |
| B. | 该品牌的矿泉水一定呈酸性 | |
| C. | “锶、钠、钙、镁、钾”属于金属元素 | |
| D. | 饮用该矿泉水可以为人体补充人体所需的无机盐 |
18.下列关于水的性质叙述,不正确的是( )
| A. | 纯净的水是没有颜色、没有气味、没有味道的液体 | |
| B. | 水的凝固是0℃,沸点是100℃ | |
| C. | 水在4℃时密度最大,为1克/厘米3 | |
| D. | 水通常较稳定,在高温或通电时才分解 |