题目内容
19.某化学兴趣小组的同学在教师的指导开展如下探究活动.(一)推断:某白色固体粉末甲可能含有硫酸铜、碳酸钠、氢氧化钠、氯化钠、硫酸钠中的一种或几种,为探究它们的组成,开展了以下实验.
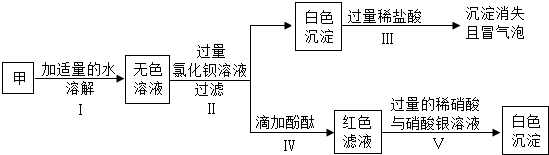
(1)甲加水后形成无色溶液的pH大于7(填“大于”、“小于”或“等于”);
(2)加水形成无色溶液说明固体甲一定不含硫酸铜,
(3)将上述框图中某试剂稍作改动,可以证实可能有的物质不存在,改动操作及不存在该物质的现象为过量的氯化钡改为过量的硝酸钡溶液,步骤Ⅴ中无明显现象.
(二)除杂:乙溶液中主要含有氯化钠、还含有少量的氯化钙、氯化镁、硫酸钠杂质,现欲提纯氯化钠开展以下实验.

(4)过量稀盐酸的作用是去除过量的氢氧化钠与碳酸钠.
(5)若“过量氯化钡溶液”与“过量固体甲”颠倒位置添加,则最后溶液中含有的溶质一定是氯化钡、氯化钠、氯化氢.
(6)最后得到的产品中所含氯化钠的质量>溶液乙中氯化钠的质量(填“>”“<”或“=”)
分析 本题能使同学们体会到实验探究的一般过程,通过实验分析可知:甲加水后形成无色溶液的pH大于7,因为加酚酞后变成红色;加水形成无色溶液说明固体甲一定不含硫酸铜,因为硫酸铜溶液是蓝色的;将上述框图中某试剂稍作改动,可以证实可能有的物质不存在,改动操作及不存在该物质的现象为:过量的氯化钡改为过量的硝酸钡溶液,步骤Ⅴ中无明显现象.除杂实验中,过量稀盐酸的作用是去除过量的氢氧化钠与碳酸钠;若“过量氯化钡溶液”与“过量固体甲”颠倒位置添加,则最后溶液中含有的溶质一定是氯化钡、氯化钠、氯化氢;最后得到的产品中所含氯化钠的质量大于溶液乙中氯化钠的质量,因为又生成了氯化钠.
解答 解:(1)通过实验分析可知:甲加水后形成无色溶液的pH大于7,因为加酚酞后变成红色;故答案为:大于;
(2)加水形成无色溶液说明固体甲一定不含硫酸铜,因为硫酸铜溶液是蓝色的;故答案为:硫酸铜;
(3)将上述框图中某试剂稍作改动,可以证实可能有的物质不存在,改动操作及不存在该物质的现象为:过量的氯化钡改为过量的硝酸钡溶液,步骤Ⅴ中无明显现象;故答案为:过量的氯化钡改为过量的硝酸钡溶液,步骤Ⅴ中无明显现象;
(4)除杂实验中,过量稀盐酸的作用是去除过量的氢氧化钠与碳酸钠;故答案为:去除过量的氢氧化钠与碳酸钠;
(5)若“过量氯化钡溶液”与“过量固体甲”颠倒位置添加,则最后溶液中含有的溶质一定是氯化钡、氯化钠、氯化氢;故答案为:氯化钡、氯化钠、氯化氢;
(6)最后得到的产品中所含氯化钠的质量大于溶液乙中氯化钠的质量,因为又生成了氯化钠,故答案为:>.
点评 实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

| A. | 延展性 | B. | 导电性 | C. | 抗腐蚀性 | D. | 导热性 |
| A. | 将23gNa投入到100g36.5%的盐酸中,所得溶液的溶质质量分数约为48% | |
| B. | 食品包装袋内的防腐剂、干燥剂和抗氧化剂等都是有害、有毒物质 | |
| C. | 电解水产物H2和O2的质量比为1:8,得出水分子中H、O元素个数比为2:1 | |
| D. | 葡萄糖分子式为C6H12O6,可以改写成C6(H12O6),所以葡萄糖由C和H2O组成 |
| A. | 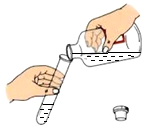 倾倒液体 | B. | 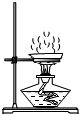 蒸发 | C. | 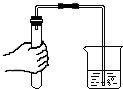 检查装置气密性 | D. | 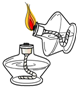 点燃酒精灯 |
| A. | 一定含有硅元素、氟元素 | B. | 可能含有氧元素 | ||
| C. | 可能含有氢元素 | D. | X是一种氧化物 |
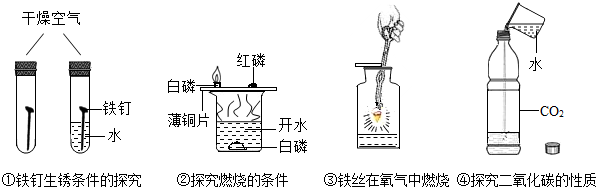
| A. | 实验①中的水:使铁生锈的条件之一 | B. | 实验②中的水:只为了提供能量 | ||
| C. | 实验③中的水:防止集气瓶炸裂 | D. | 实验④中的水:作反应物 |
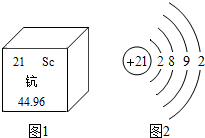 钪是稀土金属,主要用于航天合金材料.
钪是稀土金属,主要用于航天合金材料.