题目内容
10.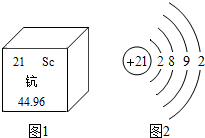 钪是稀土金属,主要用于航天合金材料.
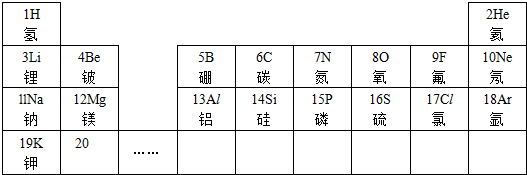
钪是稀土金属,主要用于航天合金材料.(1)图1是钪元素在元素周期表中相关信息,则钪元素的相对原子质量是44.96;图2是钪原子的结构示意图,可获取的一条信息是钪原子核内有21个质子.
(2)用化学符号表示:
①钪单质:Sc;②+3价钪的氧化物:Sc2O3.
(3)钪合金可能具有的一条性质:抗腐蚀性能高.
分析 (1)根据元素周期表和原子结构示意图的信息来分析;
(2)根据金属单质与氧化物的化学式的写法来分析;
(3)根据合金的用途来分析其性质.
解答 解:(1)由元素周期表的信息可知,钪元素的相对原子质量是44.96;从图2可知,其核电荷数为21,核外有4个电子层,最外层有2个电子等.故填:44.96;钪原子核内有21个质子(答案合理即可);
(2)金属单质是由原子直接构成的,所以其化学式用元素符号直接来表示,钪单质的化学式为Sc;
氧元素显-2价,故+3价钪的氧化物的化学式为Sc2O3;故填:Sc;Sc2O3;
(3)钪合金可用于航空、航天,说明其密度小,硬度大,抗腐蚀性能高,故填:抗腐蚀性能高(答案合理即可).
点评 本题难度不大,掌握粒子结构示意图的含义、灵活运用元素周期表中元素的信息是正确解答本题的关键.

练习册系列答案
相关题目
1.下列变化属于化学变化的是( )
| A. | 石油分馏得到汽油,煤油等 | B. | 燃放烟花 | ||
| C. | 活性炭吸附冰箱内异味 | D. | 工业分离液态空气制氧气 |
5.PM2.5是指2.5微米以下的颗粒物,主要来自化石燃料的燃烧.下列行为现象容易引起PM2.5监测指数升高的是( )
| A. | 燃煤发电 | B. | 垃圾深埋 | C. | 污水排放 | D. | 白色污染 |
20.下列实验操作正确的是( )
| A. | 用托盘天平称量固体时,应将药品放在右盘上,砝码放在左盘上 | |
| B. | 将滴瓶上的胶头滴管用后也要洗涤 | |
| C. | 可以在量筒内配制溶液 | |
| D. | 用胶头滴管时,滴管要在试管口的上方垂直滴入 |
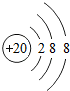 表示的是Ca2+(写粒子符号).
表示的是Ca2+(写粒子符号).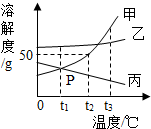 如图为甲、乙、丙三种物质的溶解度曲线示意图,请回答:
如图为甲、乙、丙三种物质的溶解度曲线示意图,请回答: