题目内容
9.已知Fe元素在化合物里通常显+2或+3价.因此Fe3O4可写成氧化物形式(FeO•Fe2O3)或盐的形式(Fe(Fe2O2)2)Pb在化合物里显+2价成+4价.那么Pb3O4化合物.也可以写成2PbO•PbO2或Pb2PbO4(写化学式)分析 分析Fe3O4 的两种书写形式中铁元素的化合价及对应化合价原子的个数,根据化合价代数和为零的原则,将规律引用到Pb3O4中,先根据其化合价写出两种氧化物的化学式,然后根据元素守恒确定其氧化物形式和盐的形式.
解答 解:Pb在化合物里显+2价或+4价,根据化合价代数和为零的原则写出Pb的两种氧化物形式为:PbO和PbO2,那么Pb3O4的氧化物的表示形式可以写成 2PbO•PbO2;盐的形式可以写成Pb2PbO4.
故答案为:2PbO•PbO2;Pb2PbO4.
点评 学会从题目中获取信息,并对信息进行处理、理解并对所获取的知识进行迁移的能力.

练习册系列答案
相关题目
20.生产、生活离不开化学知识.下列做法或行为中,正确的是( )
| A. | 用粮食酿造的米醋作调味剂 | |
| B. | 杜绝吃含有化学物质的食品 | |
| C. | 随意进入废弃的矿洞内游玩 | |
| D. | 在不通风的澡室里用燃气热水器洗澡 |
17.对二甲苯(简称PX)的化学式是C8H10,无色透明液体,具有芳香气味,可燃,其蒸气与空气可形成爆炸性混合物.下列有关对二甲苯的说法中,正确的是( )
| A. | 对二甲苯属于有机高分子化合物 | |
| B. | 对二甲苯中碳元素的质量分数大于甲烷中碳元素的质量分数 | |
| C. | 对二甲苯是由8个碳原子和10个氢原子构成 | |
| D. | 对二甲苯中碳元素、氢元素的质量比为4:5 |
1.化学是一门以实验为基础的科学,借助科学的实验方法,我们可以从不同角度正确地认识物质.
(1)探究微粒的性质:如图1所示,烧杯B中的现象是由无色液体变红色;,产生这一现象体现了分子的性质为分子不断地运动;
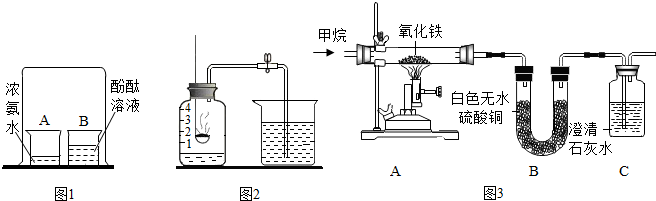
(2)探究物质的组成:图2所示实验可用于测定空气的组成.实验中能说明空气中氧气含量为五分之一的现象为:红磷燃烧结束后,冷却到室温,打开止水夹,烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)探究物质的性质:小军按图3探究甲烷的性质,他查阅资料获知白色无水硫酸铜遇水会变蓝,请完成下面的实验报告:
(1)探究微粒的性质:如图1所示,烧杯B中的现象是由无色液体变红色;,产生这一现象体现了分子的性质为分子不断地运动;

(2)探究物质的组成:图2所示实验可用于测定空气的组成.实验中能说明空气中氧气含量为五分之一的现象为:红磷燃烧结束后,冷却到室温,打开止水夹,烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)探究物质的性质:小军按图3探究甲烷的性质,他查阅资料获知白色无水硫酸铜遇水会变蓝,请完成下面的实验报告:
| 实 验 现 象 | 实 验 结 论 |
| A中红色粉末变为黑色; B中白色无水硫酸铜变蓝色; C中澄清石灰水变浑浊. | 反应的产物为二氧化碳、水, 甲烷具有还原性,A中反应的化学方程式为 3CH4+4Fe2O3$\frac{\underline{\;高温\;}}{\;}$8Fe+6H2O+3CO2 |
18.空气中那种成分会使食物变质( )
| A. | 氮气 | B. | 氧气 | C. | 水蒸气 | D. | 二氧化碳 |
19.下列有关氧气实验的说法正确的是( )
| A. | 加热分解KClO3制氧气未加MnO2 | |
| B. | 电解水实验产生氧气的电极为负极 | |
| C. | 收集氧气时,用带火星的木条进行验满,这是利用了氧气的可燃性 | |
| D. | 铁丝在氧气中燃烧,火星四射,得到黑色固体物质 |

 同学们到化学实验做实验时,常常闻到刺鼻难闻的气味,这是由于化学实验室要排放成分复杂的污染物.某校化学兴趣小组的同学在甲实验室中进行氧气分别与碳,硫,铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔气泡的作用是增大气体与溶液的接触面积,使反应充分进行).
同学们到化学实验做实验时,常常闻到刺鼻难闻的气味,这是由于化学实验室要排放成分复杂的污染物.某校化学兴趣小组的同学在甲实验室中进行氧气分别与碳,硫,铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔气泡的作用是增大气体与溶液的接触面积,使反应充分进行).