题目内容
20.生产、生活离不开化学知识.下列做法或行为中,正确的是( )| A. | 用粮食酿造的米醋作调味剂 | |
| B. | 杜绝吃含有化学物质的食品 | |
| C. | 随意进入废弃的矿洞内游玩 | |
| D. | 在不通风的澡室里用燃气热水器洗澡 |
分析 A、根据米醋中含有醋酸进行分析判断.
B、根据食品中都含有化学物质进行分析判断.
C、根据废弃的矿洞可能含有较多的二氧化碳进行分析判断.
D、根据燃气燃料不充分燃烧,会生成有毒的一氧化碳气体进行分析判断.
解答 解:A、米醋中含有醋酸,是一种常用的调味品,故选项做法正确.
B、任何食品中都含有化学物质,故选项做法错误.
C、废弃的矿洞可能含有较多的二氧化碳,进入废弃的矿洞之前,先做灯火试验,检验里面二氧化碳的浓度,故选项做法错误.
D、在不通风的澡室里用燃气热水器洗澡时,可燃物就会发生不完全燃烧而产生有剧毒的一氧化碳,可能会造成一氧化碳中毒,故选项做法错误.
故选:A.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.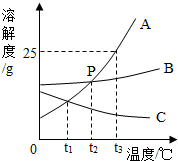 如图是A、B、C三种物质的溶解度曲线,
如图是A、B、C三种物质的溶解度曲线,
①A物质在t3℃时溶解度为25g.
②P点表示t2℃时,A、B物质的溶解度相等.
③t3℃时,把15gA物质放入50克水中充分溶解,所得溶液的质量为62.5克.
 如图是A、B、C三种物质的溶解度曲线,
如图是A、B、C三种物质的溶解度曲线,①A物质在t3℃时溶解度为25g.
②P点表示t2℃时,A、B物质的溶解度相等.
③t3℃时,把15gA物质放入50克水中充分溶解,所得溶液的质量为62.5克.
12.二氧化碳与二氧化硫同为非金属氧化物,某兴趣小组用类比法进行如下探究:
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.
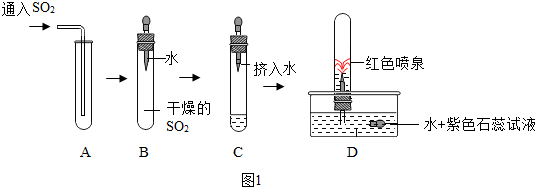
通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.
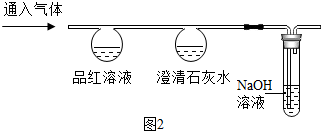
(3)由实验可知:
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
(4)测定步骤:
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.

通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.

| 实验Ⅰ | 实验Ⅱ | |
| 通入CO2 | 通入SO2 | |
| 品红溶液 | 无明显变化 | 红色褪为无色 |
| 澄清石灰水 | 白色浑浊 | 白色浑浊 |
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
| SO2最高浓度限值(单位mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
10.除去下列物质中的少量杂质(括号内为杂质),所用试剂和方法不正确的是( )
| A. | CO2(CO)-点燃 | |
| B. | KNO3(NaCl)-降温结晶 | |
| C. | NaCl溶液(Na2SO4)-加入适量的BaCl2溶液,过滤 | |
| D. | ZnSO4溶液(CuSO4)-加入过量的锌粉,过滤 |
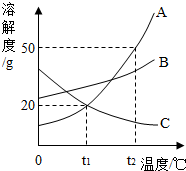 如图为A、B、C三种固体物质的溶解度曲线,请回答
如图为A、B、C三种固体物质的溶解度曲线,请回答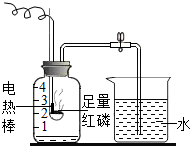 如图所示的是初中化学中的一个重要实验.请回答下列问题:
如图所示的是初中化学中的一个重要实验.请回答下列问题: