题目内容
2.下列是初中化学中的一些重要实验.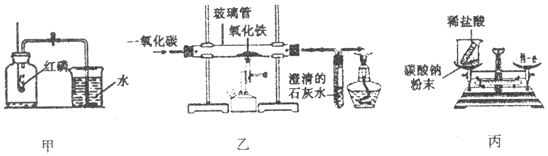
(1)甲中红磷必须足量的原因是将集气瓶中的氧气耗尽.
(2)乙中玻璃管内反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)将73g稀盐酸与106g Na2CO3粉末按丙图放好并调整天平平衡后,让两者充分反应,再在左侧托盘中加入44g砝码,在不考虑CO2溶于水及与其他物质反应的情况下,天平指针将指向表盘左侧(填“左侧”、“右侧”或“正中”).
分析 (1)测定空气中氧气的含量的原理是利用物质燃烧消耗装置内的氧气,据此进行分析解答.
(2)根据化学反应的原理以及化学方程式的写法来分析;
(3)根据化学方程式进行来分析.
解答 解:(1)该实验主要是利用物质燃烧消耗装置内的氧气,然后根据进入水的体积,判断氧气的体积.只有加入过量的红磷,才能将将氧气完全消耗掉,如果红磷的量不足,会导致实验的结果是水倒流不足五分之一.故填:将集气瓶中的氧气耗尽;
(2)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳;故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)在烧杯中会发生如下反应Na2CO3+2HCl═2NaCl+H2O+CO2↑.
106 73 44
但是题干中稀盐酸的质量为73g,则生成的二氧化碳的质量不足44g,所以在左侧托盘中加入44g砝码,左盘偏重,天平指针将指向表盘左侧;故填:左侧.
点评 本题难度不大,掌握测定空气中氧气的含量的原理、铁的冶炼、质量守恒定律等是正确解答本题的关键.

练习册系列答案
相关题目
17.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在pH=l 的溶液中:Na+、NO3-、CO32- | |
| B. | 能使石蕊变红的溶液中:K+、NH4+、Cl- | |
| C. | 在硫酸铜溶液中:Ba2+、Zn2+、CO32- | |
| D. | 在碳酸氢铵溶液中:K+、OH-、NO3- |
18.某转化过程可表示为:6CO2+6H2O$?_{呼吸作用}^{光照(光合作用)}$C6H12O6+6O2.下列叙述不正确的是( )
| A. | 葡萄糖属于糖类 | |
| B. | 适当提高CO2的浓度有利于植物的光合作用 | |
| C. | 转化过程中涉及三种氧化物 | |
| D. | 无机物和有机物可以相互转化 |
10.如图所示实验操作正确的是( )
| A. |  稀释浓硫酸 稀释浓硫酸 | B. |  读液体体积 | C. |  引燃酒精灯 | D. |  检查气密性 |
 水是生命之源,是自然界中重要的物质.
水是生命之源,是自然界中重要的物质.