题目内容
13. 如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:
如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:某碳酸钠样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11g,放入烧杯中加水完全溶解后,滴加上述配制的稀盐酸至完全反应,最后测得生成气体的质量为4.4g.计算:
(1)样品中碳酸钠的溶质质量分数(结果精确到0.1%).
(2)用去稀盐酸的质量是多少克?
分析 根据碳酸钠和盐酸反应的化学方程式,已知二氧化碳的质量为4.4g,可求出参加反应的碳酸钠的质量和氯化氢的质量.从而求出纯碱样品中碳酸钠的质量分数.
解答 解:设碳酸钠的质量为x,消耗掉的盐酸溶液的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y×10% 4.4g
$\frac{106}{x}=\frac{73}{y×10%}=\frac{44}{4.4g}$
x=10.6g;y=73g
纯碱样品中碳酸钠的质量分数为$\frac{10.6g}{11g}$×100%=96.4%
答:(1)纯碱样品中碳酸钠的质量分数为96.4%;
(2)用去稀盐酸的质量为73 g.
点评 本题难度不是很大,掌握利用化学方程式进行计算的方法是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列生活中常见的变化,一定发生化学变化的是( )
| A. | 葡萄酿酒 | B. | 石蜡熔化 | C. | 胆矾碾碎 | D. | 酒精挥发 |
8.下列实验操作错误的是( )
| A. | 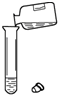 倾倒液体 | B. | 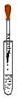 滴加液体 | C. | 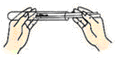 用药勺取用粉末 | D. | 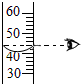 读取液体体积 |
18.2015年6月5日世界环境日中国主题是“践行绿色生活”.下列行为与此主题不相符的是( )
| A. | 提倡使用太阳能电池等绿色环保电池 | |
| B. | 将废旧电池深埋,避免重金属污染 | |
| C. | 尽可能少使用一次性的纸杯、餐具 | |
| D. | 使用微生物降解塑料和光降解塑料,减少“白色污染” |
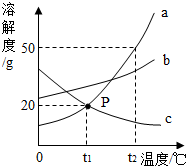 如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答: