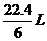29.(11分)(08年广东化学·22)
铜在自然界存在于多种矿石中,如:
|
矿石名称 |
黄铜矿 |
斑铜矿 |
辉铜矿 |
孔雀石 |
|
主要成分 |
CuFeS2 |
Cu5FeS4 |
Cu2S |
CuCO3·Cu(OH)2 |
请回答下列问题:
(1)上表所列铜化合物中,铜的质量百分含量最高的是 。
(2)工业上以黄铜矿为原料。采用火法溶炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+Cu2S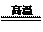 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。
(3)SO2尾气直接排放到大气中造成环境污染的后果是 ;处理该尾气可得到有价值的化学品,写出其中1种酸和1种盐的名称 。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。请简述粗铜电解得到精铜的原理: 。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母)。
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
判断 |
|
A |
铜绿的主成分是碱酸铜 |
可用稀盐酸除铜器表面的铜绿 |
Ⅰ对;Ⅱ对;有 |
|
B |
铜表易形成致密的氧化膜 |
铜容器可以盛放浓硫酸 |
Ⅰ对;Ⅱ对;有 |
|
C |
铁比铜活泼 |
例在铜板上的铁钉在潮湿空气中不易生锈 |
Ⅰ对;Ⅱ对;有 |
|
D |
蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 |
硫酸铜溶液可用作游泳池的消毒剂 |
Ⅰ错;Ⅱ对;无 |
27.(07年山东理综·29)(15分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应 负投反应 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Fe2+ |
7.0 |
9.0 |
|
Cu2+ |
4.7 |
6.7 |
|
提供的药品:Cl2
浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式
劣质不锈钢腐蚀的实验现象
答案:(1)2Fe3++Cu=2Fe2++Cu2+
(2)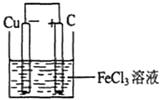
正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)
负极反应:Cu=2Cu2++2e-(或Cu-2e-=Cu2+)
(3)①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2-4.7;③过滤(除去Fe(OH)3)
(4)CuO+H2SO4=CuSO4+H2O CuSO4+Fe=FeSO4+Cu
不锈钢表面有紫红色物质生成
解析:(1)Fe3+具有强氧化性,可以把一些金属单质如铁、铜等氧化成相应的离子,Fe3+腐蚀铜制电路板利用的就是这个原理,反应的离子方程式是:2Fe3+ + Cu====2Fe2+ + Cu2+。
(2)由反应2Fe3+ + Cu====2Fe2+ + Cu2+可以判断出铜化合价升高,发生氧化反应,铜做负极,铁元素化合价降低,Fe3+ 发生还原反应,正极可以选用石墨棒,电解质溶液可以选用氯化铁溶液。回忆并仿照教材上的铜锌原电池装置,可以画出此原电池的装置图,装置图见答案。发生的电极反应为:
正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)
负极反应:Cu=2Cu2++2e-(或Cu-2e-=Cu2+)。
(3)除杂时,要把杂质全部除去,又不能引入新的杂质。根据题给信息可知:Fe3+的氢氧化物从开始沉淀到沉淀完全的pH范围是1.9-3.2,Fe2+的氢氧化物从开始沉淀到沉淀完全的pH范围是7.0-9.0,Cu2+的氢氧化物从开始沉淀到沉淀完全的pH范围是4.7-6.7。当pH为3.2时Fe3+完全沉淀,此时Cu2+不会沉淀,要使Fe2+完全沉淀需要使溶液的pH为9.0,此时Cu2+已经完全沉淀。因此,若要除去CuCl2溶液中的Fe3+、Fe2+,需要将Fe2+全部转化为Fe3+,采取的措施是向溶液中同入过量的氯气;为了不引入其它杂质,可以向溶液中加入CuO调节溶液的pH范围在3.2-4.7之间,此时Fe3+完全沉淀;最后过滤,即可得到纯净的氯化铜溶液。实验步骤见答案。
(4)不锈钢在某些盐溶液中比在酸溶液中腐蚀明显,说明这些盐溶液中的金属阳离子的氧化性比H+的氧化性强,即这些金属在金属活动性顺序位于氢的后面。要设计实验验证劣质不锈钢易被腐蚀,需要有容易与铁反应的盐,根据提供的药品可知这种盐是硫酸铜,制取硫酸铜的最佳方案是用氧化铜与稀硫酸反应制取,这种方法比浓硫酸与铜反应节省硫酸,并且不产生污染环境的SO2 。实验步骤是:①用适量水将浓硫酸稀释制取稀硫酸,②用氧化铜与稀硫酸反应制取硫酸铜,③将不锈钢加入硫酸铜溶液中观察现象。有关化学方程式和实验现象见答案。
25.(07年广东化学·24)(10分)
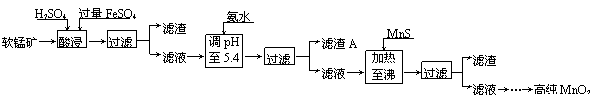 二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
CuS |
ZnS |
MnS |
FeS |
|
pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
≥–0.42 |
≥2.5 |
≥7 |
≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为 。
(2)滤渣A的主要成分是 。
(3)加入MnS的目的是除去 杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为 。
(5)从废旧碱性锌锰电池中可以回收利用的物质有 (写出两种)。
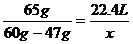 ,解得 x=4.5L。
,解得 x=4.5L。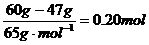 ,因为锌发生氧化反应时Zn-2e-=Zn2+,所以通过导线的电量为0.20mol×2×6.02×1023mol-1×1.60×10-19C=3.8×104C。
,因为锌发生氧化反应时Zn-2e-=Zn2+,所以通过导线的电量为0.20mol×2×6.02×1023mol-1×1.60×10-19C=3.8×104C。
 .(09年江苏化学·5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是
.(09年江苏化学·5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是 Al(OH)3(胶体)+3H+,利用Al(OH)3(胶体)的吸附性进行净水;B项,是因为轮船主要用铁造外壳,铁在海水中易被腐蚀.镀上比铁活泼的锌,形成原电池,锌作负极,失去电子先被腐蚀,从而起到保护铁的作用,从而可减缓船体的腐蚀速率;氧化镁的熔点是2852℃,可用于制作耐高温材料;电解MgCl2饱和溶液,发生地化学反应为MgCl2+2H2O
Al(OH)3(胶体)+3H+,利用Al(OH)3(胶体)的吸附性进行净水;B项,是因为轮船主要用铁造外壳,铁在海水中易被腐蚀.镀上比铁活泼的锌,形成原电池,锌作负极,失去电子先被腐蚀,从而起到保护铁的作用,从而可减缓船体的腐蚀速率;氧化镁的熔点是2852℃,可用于制作耐高温材料;电解MgCl2饱和溶液,发生地化学反应为MgCl2+2H2O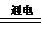 Mg(OH)2+Cl2↑+H2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2(熔融)
Mg(OH)2+Cl2↑+H2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2(熔融)
 6CO2↑+24H+
6CO2↑+24H+