网址:http://m.1010jiajiao.com/timu_id_4426757[举报]
(10分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固)  Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ·c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
(10分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性 ,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3) 已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固) ![]() Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ·c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
查看习题详情和答案>>
(10分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性 ,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3) 已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
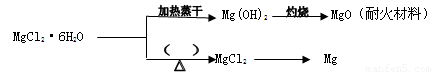
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固)  Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________
有利于Mg(OH)2溶解。
Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________
有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ·c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
查看习题详情和答案>>
试分析回答下列问题:
(1)已知汽车在刹车和下坡时,镍氢电池两电极反应分别为:甲电极:M+H2O+e-→MH+OH-(M为储氢合金,MH为吸附了氢原子的储氢合金)乙电极:Ni(OH)2+OH--e-→NiOOH+H2O则在这一过程中甲、乙两电极的名称分别是:甲:
(2)当汽车上坡或加速时,镍氢电池两电极反应分别为:甲电极:
(3)内燃机工作时因为部分汽油不完全燃烧会产生污染大气的CO,已知在常温常压下:
C8 H18(1)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5121.9kJ/mol
2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol
H2O(g)=H2 O(1);△H=-44.0kJ/mol
写出汽油不完全燃烧生成一氧化碳和液态水的热化学方程式:
| 17 |
| 2 |
| 17 |
| 2 |
(4)为降低汽车尾气中的一氧化碳的浓度,可采取在汽车的排气管上增加一个补燃器,通过下列反应来实现转化:
2CO(g)+O2(g)?2CO2(g)
已知在温度为T的条件下,当补燃器中化学反应速率V(正)=V(逆)时,各物质浓度存在下列恒定关系:
| c(CO2)2 |
| c(CO)2×c(O2) |
在温度为T的条件下,若某汽车排人补燃器的CO、CO2的浓度分别为1.0×10-5mol?L-1和1.01×10-4mol?L-1,要在该温度下使最终尾气中CO的浓度降为1.0×10-6mol?L-1,则补燃器中应不断补充O2,并使O2浓度保持在
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

写出反应②的化学方程式.
(2)试管B收集到的产品中,其中有一种物质M能使酸性高锰酸钾溶液褪色.
①试写出体现该物质重要用途的一个反应方程式


②如该物质发生一氯取代,则生成物的同分异构体共有有
③另有M的同系物,分子式为C10Hn,则n=
 、
、 、
、
 、
、 、
、
(3)锥形瓶C中观察到的现象
(4)写出C中逸出的气体在工业上的两种用途