考点1.几种重要的金属及合金
(1)金属的物理特性:常温下除汞(液体)外都是固体,有金属光泽,大多数为电和热的优良导体,有延展性、密度较大、熔点较高。
(2)几种常见金属的比较(见表8-18-1):
表8-18-1
|
金属 |
物理性质 |
用 途 |
|
铁 |
纯铁具有银白色金属光泽、质软,有良好的延展性,密度7.86g/cm3,熔点1535℃,沸点2750℃,是电和热的良导体 |
电器、建筑、工业材料,如:制造桥梁、铁轨、舰船、车辆和各种机械等 |
|
铜 |
紫红色金属,密度8.92g/cm3,熔点1083℃,沸点2595℃,具有良好的延展性、导电性、导热性 |
电线、电缆和各种电器,铜合金可用于制造各种零件等 |
|
铝 |
银白色金属,密度2.70g/cm3,熔点660℃,沸点2467℃,具有良好的延展性、导电性、导热性 |
冶炼金属,做电线、电缆,铝合金用于制造门窗、飞机等 |
(3)合金:①概念:在一种金属中加热熔合其他金属或非金属,而形成的具有金属特性的物质称为合金。②合金的性质能:合金的很多性能与组成它们的纯金属不同,使合金更易适合不同的用途,日常生活中使用的金属材料,大多数为合金。③重要的铁合金:生铁和钢都是铁的合金,其区别是含碳量不同。④生铁的含铁量为2%~4.3%,钢的含碳量为0.03%~2%。
考点2.金属与氧气的反应
大多数金属都能与氧气反应,但反应的难易和剧烈程度不同,越活泼的金属,越容易与氧气发生化学反应,反应越剧烈。
(1)镁、铝与氧气的反应:①在常温下,镁条在空气中发生缓慢氧化而生成白色固体--氧化镁,但在点燃条件下,镁条能在空气中剧烈燃烧,生成白色固钵。②在常温下,铝在空气中发生缓慢氧化,在其表面生成一层致密的氧化物薄膜,从而阻止内部的铝进一步氧化,因此,铝具有较好的抗腐蚀性;在点燃的条件下,铝在氧气中剧烈燃烧生成白色固体--氧化铝(Al2O3)。
(2)铁与氧气的反应:①常温下,铁在干燥的空气中很难与氧气反应;②常温下,铁在潮湿的空气中易生锈;③在点燃的条件下,铁在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体物质--四氧化三铁。
(3)铜与氧气的反应:①常温下,铜在干燥的空气中几乎不与氧气反应;②铜在空气中加热时,表面会逐渐生成黑色物质--氧化铜;③铜在潮湿的空气中易形成铜绿(碱式碳酸铜)。
(4)金、铂即使在高温下也不与氧气反应。
考点3.金属活动性顺序及置换反应
(1)金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
(2)金属活动性顺序的作用:①判断金属与酸的反应:a. 一般说来,排在氢前面的金属能置换出酸中的氢,排在氢后面的金属不能置换出酸中的氢;b. 酸不包括浓硫酸和硝酸,因为它们有很强的氧化性,与金属反应不能生成氢气,而生成水。②判断金属与盐溶液反应。在金属活动性顺序里,只有排在前面的金属,才能把排在后面的金属从它们的盐溶液中置换出来。③判断金属活动性强弱:在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。④判断金属跟混合盐溶液反应的次序。
(3)置换反应:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应叫做置换反应。
可用式子表示:A+BC==B+AC;例如:Fe+2HCl==FeCl2+H2↑,Cu+2AgAO3==Cu(NO3)2+2Ag。
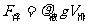 可知,只要我们改变液体的密度,则浮力就会改变,如果液体的密度变小,则浮力变小,物体要下沉;如果液体的密度变大,则浮力变大,物体要上浮。
可知,只要我们改变液体的密度,则浮力就会改变,如果液体的密度变小,则浮力变小,物体要下沉;如果液体的密度变大,则浮力变大,物体要上浮。


 (2)不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液。
(2)不饱和溶液:在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液。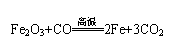 (2)铁的冶炼:①原理:利用高温条件下,焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来。如用赤铁矿石炼铁的化学方程式为:
。②原料:铁矿石、焦炭、石灰石及空气。③设备:高炉。④炼铁时选择铁矿石的标准:a.铁矿石中铁元素的质量分数大(即含铁量高);b.炼铁过程中产物对空气不能造成污染;满足以上两个条件的矿石是理想的绿色矿石。
(2)铁的冶炼:①原理:利用高温条件下,焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来。如用赤铁矿石炼铁的化学方程式为:
。②原料:铁矿石、焦炭、石灰石及空气。③设备:高炉。④炼铁时选择铁矿石的标准:a.铁矿石中铁元素的质量分数大(即含铁量高);b.炼铁过程中产物对空气不能造成污染;满足以上两个条件的矿石是理想的绿色矿石。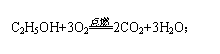 (1)乙醇:①乙醇俗称酒精,化学式为:C2H5OH;②乙醇是一种可再生的清洁能源;③乙醇具有可燃性:
④乙醇被用作酒精灯、火锅、内燃机等燃料。
(1)乙醇:①乙醇俗称酒精,化学式为:C2H5OH;②乙醇是一种可再生的清洁能源;③乙醇具有可燃性:
④乙醇被用作酒精灯、火锅、内燃机等燃料。 (1)煤和石油:①煤:a.煤是古代植物遗体在地下经过长期复杂变化形成的,是由有机物和无机物所组成的复杂混合物,主要含有碳元素,此外,还含有少量的氢、氮、硫、氧等元素。
(1)煤和石油:①煤:a.煤是古代植物遗体在地下经过长期复杂变化形成的,是由有机物和无机物所组成的复杂混合物,主要含有碳元素,此外,还含有少量的氢、氮、硫、氧等元素。 (2)石油:①石油是由古代动植物遗体在地壳中经过非常复杂的变化而形成的,是一种复杂的混合物,石油有特殊的气味,不溶于水,密度比水的稍小,没有固定的熔点和沸点。②石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素。③石油 溶剂油、汽油、煤油、柴油、润滑油、石蜡、沥青。石油不仅可以蒸馏(物理变化)得到不同沸点的成分,而且经过石油化工(化学变化)得到多种产品。
(2)石油:①石油是由古代动植物遗体在地壳中经过非常复杂的变化而形成的,是一种复杂的混合物,石油有特殊的气味,不溶于水,密度比水的稍小,没有固定的熔点和沸点。②石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素。③石油 溶剂油、汽油、煤油、柴油、润滑油、石蜡、沥青。石油不仅可以蒸馏(物理变化)得到不同沸点的成分,而且经过石油化工(化学变化)得到多种产品。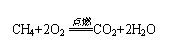 (3)天然气:①俗名:沼气、坑气;②主要成分:甲烷(CH4);③物理性质:无色无味的气体,难溶于水,密度比空气小;④化学性质:具有可燃性,
。a.点燃前必须检验纯度;b.燃烧时主要现象:发出蓝色火焰,烧杯内壁有水雾出现,烧杯内注入澄清石灰水,石灰水变浑浊。
(3)天然气:①俗名:沼气、坑气;②主要成分:甲烷(CH4);③物理性质:无色无味的气体,难溶于水,密度比空气小;④化学性质:具有可燃性,
。a.点燃前必须检验纯度;b.燃烧时主要现象:发出蓝色火焰,烧杯内壁有水雾出现,烧杯内注入澄清石灰水,石灰水变浑浊。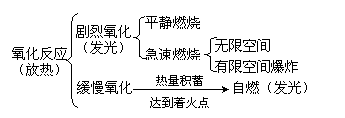 (3)四者的关系如下:
(3)四者的关系如下: