考点1.二氧化碳的性质和用途
|
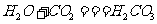 ,碳酸能使紫色石蕊试液变红。碳酸不稳定,受热易分解,
,碳酸能使紫色石蕊试液变红。碳酸不稳定,受热易分解,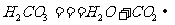 ③二氧化碳和澄清石灰水反应:二氧化碳和澄清石灰水中的氢氧化钙反应,生成不溶于水的白色物质碳酸钙,使澄清的石灰水变浑浊,
③二氧化碳和澄清石灰水反应:二氧化碳和澄清石灰水中的氢氧化钙反应,生成不溶于水的白色物质碳酸钙,使澄清的石灰水变浑浊,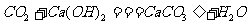 ,利用此反应可以鉴定CO2的存在。(3)二氧化碳的用途:①可用于灭火;②做制冷剂、人工降雨;③制汽水;④可用作温室肥料;⑤重要的化工原料,制纯碱、尿素等。
,利用此反应可以鉴定CO2的存在。(3)二氧化碳的用途:①可用于灭火;②做制冷剂、人工降雨;③制汽水;④可用作温室肥料;⑤重要的化工原料,制纯碱、尿素等。
考点2.二氧化碳的实验室制法
(1)药品:石灰石(或大理石)和稀盐酸。(2)反应原理:CaCO3+2HCl==CaCl2+CO2↑+H2O。(3)实验装置:类似于制氢气的装置,因为实验室制取CO2是常温下用固体和液体反应制得的。(4)收集方法:因为CO2能溶于水,不能用排水法收集;CO2的密度比空气大,可用向上排空气法收集。(5)检验方法:验证:把制得的气体通入澄清石灰水中,若澄清石灰水变浑浊,证明这种无色气体是CO2。验满:把燃着的木条放在集气瓶口,若火焰熄灭,证明瓶内已充满CO2。(6)注意:实验室制取CO2不能用碳酸钠代替大理石(或石灰石),原因是反应速率太快,不宜收集;不能用浓盐酸代替稀盐酸,原因是浓盐酸易挥发,使收集的CO2气体中混有较多氯化氢气体;也不能用稀硫酸代替稀盐酸,原因是生成的CaSO4微溶于水,覆盖在大理石(或石灰石)表面,阻止反应续续进行。
考点1.碳的几种单质的性质和用途
(1)金刚石和石墨的物理性质和用途(见表6-14-1):
表6-14-1
|
物质 |
金刚石 |
石墨 |
|
|
物 理 性 质 |
色、态 |
无色透明正八面体形状的固体,琢磨后有夺目光泽 |
深灰色不透明细鳞片状的固体,有金属光泽 |
|
硬度 |
最硬的矿物之一(坚硬) |
最软的矿物之一(质软) |
|
|
熔点 |
高 |
高 |
|
|
导电性 |
不导电 |
良好 |
|
|
导热性 |
不导热 |
良好 |
|
|
用途 |
钻头、划玻璃、装饰品 |
电极、润滑剂、铅笔芯 |
(2)无定形碳:①构成:无定形碳都是由石黑的微小晶体和少量杂质构成的,无定形碳都是混合物。②分类:无定形碳包括木炭、活性炭、焦炭和炭黑四种。③用途:木炭和活性炭具有吸附作用,能把大量的气体或染料等微小粒子吸附在它的表面,活性炭的吸附作用比木炭强,防毒面具里的滤毒罐就是利用活性炭来吸附毒气的,制糖工业中利用活性炭来脱色以制白糖;焦炭常用于冶金工业,用于冶炼生铁;炭黑常用于制造墨、油墨、油漆、鞋油和颜料等。
(3)碳的化学性质:在常温下,碳的化学性质不活泼,表现出稳定性,随着温度升高,化学活动性大大增强,表现出可燃性和还原性。①可燃性:a. 碳与充足的氧气反应: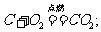
b. 碳不充分燃烧时: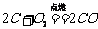 。②还原性: a. 碳还原氧化铜:
。②还原性: a. 碳还原氧化铜: 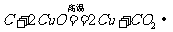 。现象:黑色粉末逐渐变成红色,产生的气体能使澄清的石灰水变浑浊;b.碳还原二氧化碳:
。现象:黑色粉末逐渐变成红色,产生的气体能使澄清的石灰水变浑浊;b.碳还原二氧化碳: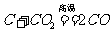 。
。
考点2.一氧化碳的性质和用途
(1)一氧化碳的物理性质:一氧化碳通常是无色、无味、有毒的气体,密度比空气略小,难溶于水。
|
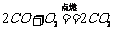 ;c. 注意:点燃一氧化碳前要验纯。②还原性;一氧化碳能将CuO(金属氧化物)还原成铜,同时生成二氧化碳:CO+CuO == Cu+CO2,因此一氧化碳可用于冶金工业。
;c. 注意:点燃一氧化碳前要验纯。②还原性;一氧化碳能将CuO(金属氧化物)还原成铜,同时生成二氧化碳:CO+CuO == Cu+CO2,因此一氧化碳可用于冶金工业。
(3)一氧化碳还原氧化铜的实验。操作顺序:与H2还原CuO的实验操作顺序一样,先通CO,再加热;实验完毕,先停止加热,继续通CO至试管冷却。尾气处理:因CO有剧毒,不能随意排入空气中,处理的基本原则是将CO燃烧掉,转化为无毒的CO2或收集备用。
(4)一氧化碳的毒性、产生方式及用途:①一氧化碳的毒性:CO和人体血红蛋白的结合力比氧与血红蛋白的结合力强,人吸入CO会造成人体缺氧,严重者会致死。②产生CO的三种主要方式:a. 氧气的量不足,碳燃烧不充分:③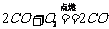 ;b. CO2遇到炽热的碳;
;b. CO2遇到炽热的碳;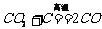 ;c. 碳与水蒸气高温条件下反应:
;c. 碳与水蒸气高温条件下反应: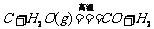 (水煤气)。③一氧化碳的用途:CO具有可燃性,可作燃料;CO具有还原性,可用来冶炼金属,如炼铁等。
(水煤气)。③一氧化碳的用途:CO具有可燃性,可作燃料;CO具有还原性,可用来冶炼金属,如炼铁等。
 (1)爆炸:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。(2)易燃物、易爆物的安全知识:一般来说,易燃物指的是那些易燃的气体和液体,容易燃烧、自然或遇火可以燃烧的固体以及一些可以引起其他物质燃烧的物质等。易爆物指的是那些受热或受到撞击时容易发生爆炸的物质等。易燃物和易爆物在遇到明火、高温或撞击时,极易燃烧或发生爆炸。因此,在生产、运输、使用和贮存易燃物和易爆物时,必须严格遵守有关规定,绝不允许违章操作。(3)一些与燃烧和爆炸有关的图标如图7-16-3所示:
(1)爆炸:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。(2)易燃物、易爆物的安全知识:一般来说,易燃物指的是那些易燃的气体和液体,容易燃烧、自然或遇火可以燃烧的固体以及一些可以引起其他物质燃烧的物质等。易爆物指的是那些受热或受到撞击时容易发生爆炸的物质等。易燃物和易爆物在遇到明火、高温或撞击时,极易燃烧或发生爆炸。因此,在生产、运输、使用和贮存易燃物和易爆物时,必须严格遵守有关规定,绝不允许违章操作。(3)一些与燃烧和爆炸有关的图标如图7-16-3所示:
 。
。 。
。