4、现有氧化铜和碳粉的混合物共Amol,将它在隔绝空气条件下加热,反应完全后,冷却,得到残留固体。
(1)写出可能发生反应的化学方程式
(2)若氧化铜在混合物中的量的比值为x(0<x<1)
问:x为何值时,残留固体为何种物质?写出残留固体的物质的量与x值之间 的关系。将结果填入下表。
|
|
残 留 固 体 |
|
|
x值 |
分子 式 |
物质的量 |
|
|
|
|
解析:(1)首先写出有关的化学反应方程式,根据化学方程式中有关物质间的物质的量的关系,分析当CuO恰好完全反应时,x值是多少?
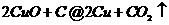 ①
①
 ②
②
按①式反应,x值为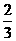 时,反应物恰好反应;按②式反应,x值为
时,反应物恰好反应;按②式反应,x值为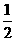 时,反应物恰好完全反应。
时,反应物恰好完全反应。
(2)当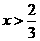 时,CuO过量,按C的量计算。
时,CuO过量,按C的量计算。

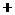
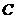

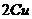
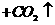
2mol 1mol 2mol
Ax A(1-x) 2A(1-x)
剩余CuO的物质的量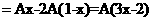
(3)当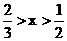 时,
时,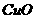 不足量,按CuO的量计算,生成铜的量为Ax。
不足量,按CuO的量计算,生成铜的量为Ax。
(4)当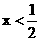 时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:
时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:
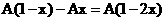
将所得结果的有关数值填入下表:
|
x 值 |
残 留 固 体 |
|
|
|
分 子 式 |
物 质 的 量 |
 |
Cu CuO |
2A(1-x) A(3x-2) |
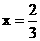 |
Cu |
Ax(或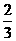 A) A) |
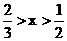 |
Cu |
Ax |
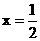 |
Cu |
Ax(或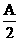 ) ) |
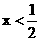 |
Cu C |
Ax A(1-2x) |
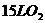 ,通入10LCO和
,通入10LCO和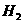 的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强
的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强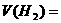
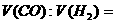 ( )
( )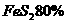 的硫铁矿生成硫酸,已知该矿石的利用率为95%,SO2的转化率为90%,SO3的吸收过程中损失率为2%,求生产500t98%的硫酸需矿石的质量和标况下空气的体积。(假设空气中氧气的体积分数为20%)。
的硫铁矿生成硫酸,已知该矿石的利用率为95%,SO2的转化率为90%,SO3的吸收过程中损失率为2%,求生产500t98%的硫酸需矿石的质量和标况下空气的体积。(假设空气中氧气的体积分数为20%)。 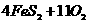

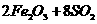 ①;
①;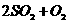
 另外,氧气参与了两个反应,可将①+②×4+③×8,整理后得出相应的关系式:
另外,氧气参与了两个反应,可将①+②×4+③×8,整理后得出相应的关系式:
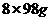
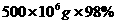
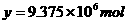
 。
。 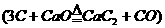 ,假设原料的利用率为95%,则36t焦炭可生产多少t乙炔?
,假设原料的利用率为95%,则36t焦炭可生产多少t乙炔?
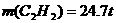
 的质量分数,称取Wg石灰石样品,加入过量的浓度为6mol/L的盐酸,使它完全溶解,加热煮沸,除去溶解的
的质量分数,称取Wg石灰石样品,加入过量的浓度为6mol/L的盐酸,使它完全溶解,加热煮沸,除去溶解的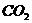 ,再加入足量的草酸铵
,再加入足量的草酸铵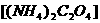 溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉淀:
溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉淀: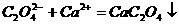 ,过滤出
,过滤出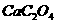 后,用稀
后,用稀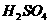 溶解:
溶解: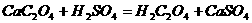 ,再用蒸馏水稀释溶液至
,再用蒸馏水稀释溶液至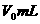 ,取出
,取出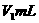 用
用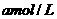 的
的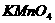 酸性溶液滴定,此时发生反应:
酸性溶液滴定,此时发生反应: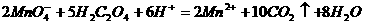 ,若滴定终点时消耗amol/L的
,若滴定终点时消耗amol/L的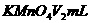 ,计算样品中
,计算样品中
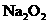 和
和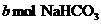 固体混合后,在密闭容器中加热到250℃,让其充分反应,假设
固体混合后,在密闭容器中加热到250℃,让其充分反应,假设 分解产生的
分解产生的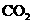 与
与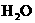 再与
再与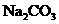 ,排出气体为
,排出气体为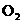 ,
,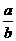 的值为________.
的值为________.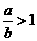 时,剩余固体为________,排出气体为________.
时,剩余固体为________,排出气体为________.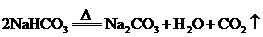 ①
① 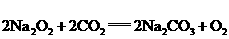 ②
② 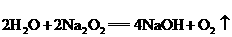 ③
③

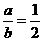 .
.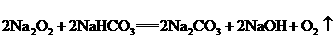
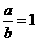 .因为有水生成,所以
.因为有水生成,所以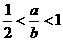
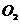 和
和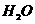 为等物质的量时,依方程式讨论有:
为等物质的量时,依方程式讨论有: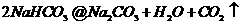
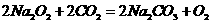
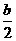
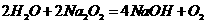
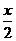
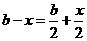
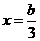
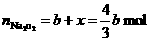 ,用去
,用去 的物质的量为:
的物质的量为: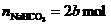
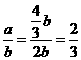
 粉末,往右盘烧杯中加入x g A物质粉末,充分反应后天平仍保持平衡.
粉末,往右盘烧杯中加入x g A物质粉末,充分反应后天平仍保持平衡.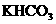 ,且两只烧杯中均无固态物质存在,则x的取值必须满足的条件是________.
,且两只烧杯中均无固态物质存在,则x的取值必须满足的条件是________.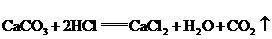 溶液增重
溶液增重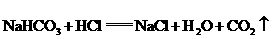 溶液增重
溶液增重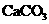 恰好完全反应时,消耗
恰好完全反应时,消耗 时;0.3 mol HCl与
时;0.3 mol HCl与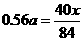 x=1.176a
x=1.176a 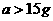 时,盐酸对于
时,盐酸对于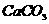 不足,且对于
不足,且对于 恰好完全反应时,加入
恰好完全反应时,加入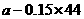 ,而加入
,而加入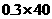 。则天平保持平衡的条件是:
。则天平保持平衡的条件是: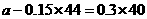
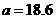
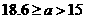 时,天平保持平衡的条件是:
时,天平保持平衡的条件是: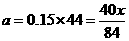
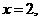
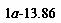
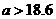 时,天平保持平衡的条件是:
时,天平保持平衡的条件是: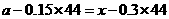
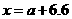
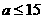 。
。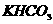 的摩尔质量相当,当等质量的
的摩尔质量相当,当等质量的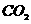 质量相等,所以天平保持平衡时:
质量相等,所以天平保持平衡时: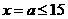
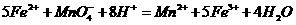 。通过计算、确定KNO3的还原产物是什么?(还原产物为氧化物)并写出其离子方程式。
。通过计算、确定KNO3的还原产物是什么?(还原产物为氧化物)并写出其离子方程式。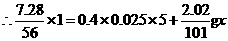
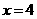
 ,还原产物为
,还原产物为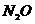
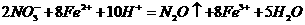
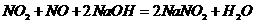 现欲用V L某烧碱溶液使由nmol NO和m mol NO2组成的混合气体中的氮全部进入溶液中,NaOH溶液的物质的量浓度至少为多少?
现欲用V L某烧碱溶液使由nmol NO和m mol NO2组成的混合气体中的氮全部进入溶液中,NaOH溶液的物质的量浓度至少为多少?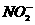 的物质的量比为1∶1,根据反应中Na+与N原子的物质的量守恒,可列出方程。
的物质的量比为1∶1,根据反应中Na+与N原子的物质的量守恒,可列出方程。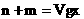
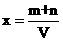 (mol/L)
(mol/L)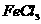 和
和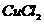 的混合溶液中,发生下列反应:
的混合溶液中,发生下列反应: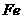
 +
+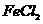
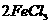
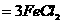
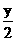 mol
ymol
mol
ymol