17.(福州三中2008-2009学年第一学期高三化学半期考)某课外兴趣小组为了探究碱性溶液中Mg2+、AlO2-与溶液pH的关系,进行下列实验:向含有0.1 mol HCl、0.1 mol MgCl2、1.0 mol AlCl3的混合溶液中逐渐加入NaOH溶液,均至反应后溶液体积1 L。测得部分实验数据如下表:
|
pH |
9 |
10 |
11 |
|
c(Mg2+)/ mol·L-1 |
10-1 |
10-3 |
10-5 |
|
c(AlO2―)/mol·L-1 |
10-2 |
10-1 |
1 |
试回答:
(1)若向混合溶液中加入NaOH溶液至pH=9,请用所给的实验数据判断,有否Mg(OH)2
沉淀出现________(填“能”或“否”),由此你得到的初步结论是__________________。
(2)若向混合溶液中加入NaOH溶液至pH=10,请写出反应各阶段所发生反应的离子
方程式__________,____________,_________________,________________,那么,所加入的NaOH溶液中溶质的的物质的量为_____________
[答案](1)否 Mg2+在弱碱性溶液中不能生成沉淀或Mg(OH)2存在溶解平衡
(2)pH =10时,溶液中c(Mg2+)=10-3mol ·L-1,c(AlO2―)=0.1 mo l·L-1
向混合溶液中加入NaOH溶液反应过程分为三个阶段:
H+ + 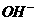 = H2O
= H2O
 C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了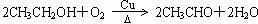 (2)CH2=CH2 + H2O → CH3CH2OH ,100%
(2)CH2=CH2 + H2O → CH3CH2OH ,100% (3)①3 ②
③BCD
(3)①3 ②
③BCD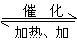 则甲烷直接将NO2还原为N2的热化学方程式为:_______________________________
则甲烷直接将NO2还原为N2的热化学方程式为:_______________________________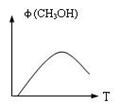 写出该反应平衡常数K=
写出该反应平衡常数K=
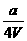 mol/L B.
mol/L B.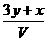 mol/L C.
mol/L C.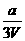 mol/L
D.无法计算
mol/L
D.无法计算