17、(16分)一包白色粉末中一定含有碳酸钠,可能还含有硫酸钠、氯化钠中的一种或两种,为进一步确认白色粉末的成份,某兴趣小组对白色粉末样品进行了探究。
可选用的仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹
可选用的药品:1.0 mol·L-1H2SO4、1.0 mol·L-1HNO3、1.0mol·L-1HCl、NaOH稀溶液、0.1 mol·L-1AgNO3、0.1 mol·L-1BaCl2 、0.1 mol·L-1Ba(NO3)2、蒸馏水。
以下是实验探究过程:
1)提出假设:
假设1 白色粉末为 的混合物;
假设2 白色粉末为 的混合物;
假设3 白色粉末为碳酸钠、硫酸钠、氯化钠的混合物;
2)基于假设设计实验方案
3)根据实验方案进行实验
请回答:
(1)某同学取少许样品于试管中,加适量蒸馏水溶解,向试管中滴入0.1 mol·L-1的BaCl2溶液,有白色沉淀产生,他认为样品中含有Na2SO4。你认为他的结论是 (填“对的”或“错的”),原因是:
(2)基于假设3,请根据实验方案,将实验操作和预期的现象及结论填入下表中:
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
|
有气体产生,说明样品中含有Na2CO3。 |
|
② |
向试管中加入0.1 mol·L-1的Ba(NO3)2
溶液。若有沉淀产生,则继续加入0.1 mol·L-1Ba(NO3)2至过量。 |
|
|
③ |
若②操作无沉淀,则向试管中加入0.1 mol·L-1AgNO3 溶液。若②操作中有沉淀,则将试管静置片刻后,取上层清液于另一去试管中,加入0.1 mol·L-1AgNO3溶液。 |
|
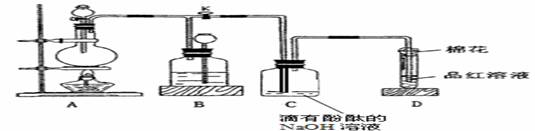
14、(16分)对于新制备的氯水进行如下实验:
|
实验 |
现象 |
相应的方程式或解释 |
|
滴入FeCl2溶液 |
|
|
|
滴入AgNO3溶液 |
|
|
|
加入CaCO3固体 |
|
|
|
滴入NaHCO3溶液 |
|
|
|
滴入紫色石蕊试液 |
|
|