17 (6分)(1)1mol/L的CaCl2 溶液0.5L,Cl- 离子的物质的量浓度为___________mol/L
(2)标准状况下,33.6L的NH3所具有的物质的量为_________mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为__________mol/L
18(8分)下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。請根据此表,结合中学学过的化学知识,回答下列问题:
|
配料表 |
精制海盐、碘酸钾(KIO3) |
|
含碘量 |
20―40mg/kg |
|
储藏方法 |
密封避光、防潮 |
|
食用方法 |
烹调时待食品熟后加入碘盐 |
(1) 据物质分类中的树状分类法有关知识,在① HIO3 ② 碘酸钠 ③ KOH
④ I2O5 ⑤ NaCl五种 (填“混合物”或“化合物”或“盐”或“氧化物”)中与碘酸钾(KIO3)属于同类物质的有 (填序号)。
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3) 溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时 。
19 (10分)实验室制配0.5 mol/L的NaOH溶液500 mL,有以下仪器:①烧杯 ②100 mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦滴定管
(1)配制时,必须使用的仪器有____________(填代号),还缺少的仪器是___ 。
(2)实验两次用到玻璃棒,其作用分别是:______________、______________。
(3)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_______________ 。
20 (16分)四只试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。
在四支试管中分别取四种溶液各1mL,做下列实验。
(1)在四支试管中分别滴入 ,出现 现象的是 离子方程式是 。
(2)在剩余三支试管中分别滴入 ,出现 现象的 离子方程式是 。
(3)在剩余两支试管中分别滴入 ,出现 现象的是 离子方程式是 。三次实验中都没有明显现象的是 。
21 (12分)已知酒精(C2H5OH)能与K2Cr2O7和H2SO4的混合物溶液发生如下反应:2 K2Cr2O7 + 3 C2H5OH + 8 H2SO4 = 2 K2SO4 + 2 Cr2(SO4) 3 + 3 CH 3COOH + 11 H2O 且知Cr2O72-和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应 (填“是”或“不是”)离子反应。
(2) 写出电离方程式:
Cr2(SO4) 3:
K2Cr2O7:
(3)该反应 (填“是”或“不是”)氧化还原反应,判断的依据是
(4)该反应能否用来检查司机是否酒后开车 (填“能”或“不能”),理由是
18. (8分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
(8分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
|
请回答:
(1)混合物中是否存在FeCl2_________(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。
(3)写出反应⑤的离子反应方程式;___________________________________。
(4)请根据图中数据分析,原固体混合物的成分为______________________(写化学式)。
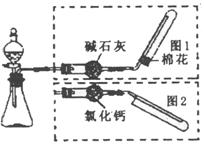
16.下图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示。下列选项中正确的是 ( )
|
|
发生装置的药品 |
干燥和集气装置 |
|
A |
氧化钙和浓氨水 |
图1 |
|
B |
大理石和稀盐酸 |
图1 |
|
C |
铜和稀硝酸 |
图2 |
|
D |
电石和水 |
图2 |
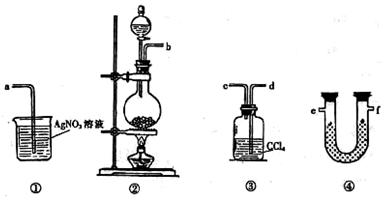
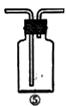
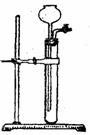 (2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是 。
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是 。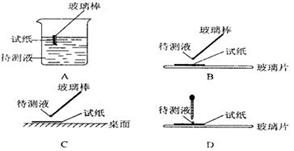
 ) 为b mol。则下列叙述中错误的是 ( )
) 为b mol。则下列叙述中错误的是 ( )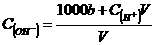 mol/L
mol/L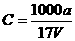 mol/L
mol/L