18、(10分)部分中学化学常见元素原子结构及性质如表所示:
|
序号 |
元素 |
结构及性质 |
|
① |
A |
A是生活中常见金属,它有两种氯化物,相对原子质量相差35.5 |
|
② |
B |
B原子最外层电子数是内层电子数和的1/5 |
|
③ |
C |
C单质分子中含化学键数最多,单质稳定,但其原子较活泼 |
|
④ |
D |
D被誉为“信息革命的催化剂”,常用的半导体材料 |
|
⑤ |
E |
通常情况下,E没有正化合价,A、B、C、D都能与E化合 |
|
⑥ |
F |
F在周期表中可以排在IA族,也有人提出排在ⅦA族、ⅣA族 |
(1)如果A与冷的浓硝酸作用发生钝化,工业上冶炼A单质的化学方程式为
____________________________________________
(2)A的氯化物的浓溶液分别滴入冷水、热水中,得到黄色和红褐色液体,区别两种液体
的方法是________________________________________________________
(3)B与C简单离子的半径大小为_________________(用离子符号表示)
(4) C和D形成的化合物的熔点很高,是一种无机非金属材料,其晶体类型为___________ ;
化学式为___________。
(5) F与E可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的
实验方法为:___________________________________________,F与C组成的两种化合物M、N,所含电子数分别与X、Y相等,请写出M的电子式___________,N的化学式___________.
(6)在上述六种元素中,选两种元素组成化合物甲,甲既含有离子键又含有共价键,甲的
化学式为___________
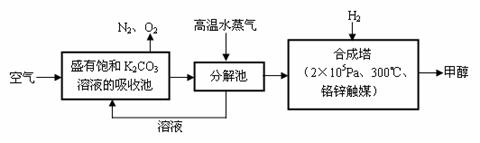 提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下: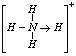 (2)N4H4(SO4)2___________(填“能”或“不能”)和草木灰混合施用。
(2)N4H4(SO4)2___________(填“能”或“不能”)和草木灰混合施用。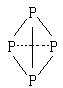 (3)已知白磷、NH4+ 、N4H44+ 的空间构型均为四面体,NH4+的结构式为
(3)已知白磷、NH4+ 、N4H44+ 的空间构型均为四面体,NH4+的结构式为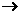 表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
表示共用电子对由N原子单方面提供),白磷(P4)的结构式为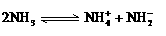 。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________________________________;
。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________________________________;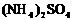 和NH3·H2O的水溶液称为“缓冲溶液”,在此溶液中加入少量的强碱或强酸时,溶液的pH几乎不变,这可由下列离子方程式来说明。
和NH3·H2O的水溶液称为“缓冲溶液”,在此溶液中加入少量的强碱或强酸时,溶液的pH几乎不变,这可由下列离子方程式来说明。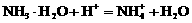 ;加碱时:
;加碱时: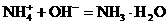
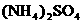 和
和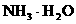 的大量存在,加少量酸或碱时,溶液中
的大量存在,加少量酸或碱时,溶液中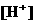 与
与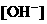 基本保持不变;
基本保持不变;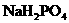 和
和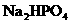 的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或强碱时发生的离子反应方程式:
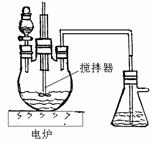
的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或强碱时发生的离子反应方程式: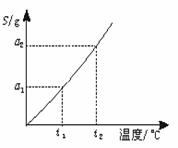 (Ⅱ)(4分) 摩尔质量为M g·mol-1的某物质溶解度曲线如右图所示,现有t2℃时300 g该物质的溶液,恒温蒸发掉50
g水后,溶液恰好达到饱和,此饱和溶液的密度为ρ g·cm-3,则其饱和溶液的物质的量浓度为
mol·L-1。若将饱和溶液降温到t1℃,析出晶体(不含结晶水)的质量为
。
(Ⅱ)(4分) 摩尔质量为M g·mol-1的某物质溶解度曲线如右图所示,现有t2℃时300 g该物质的溶液,恒温蒸发掉50
g水后,溶液恰好达到饱和,此饱和溶液的密度为ρ g·cm-3,则其饱和溶液的物质的量浓度为
mol·L-1。若将饱和溶液降温到t1℃,析出晶体(不含结晶水)的质量为
。 (3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想______________________。
(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想______________________。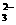 +O2+xOH-
+O2+xOH-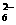 +2H2O,
+2H2O,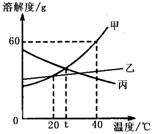 甲、乙、丙三种物质(均不含结晶水)的溶解度曲线如图所示,以下说法不正确的是
甲、乙、丙三种物质(均不含结晶水)的溶解度曲线如图所示,以下说法不正确的是