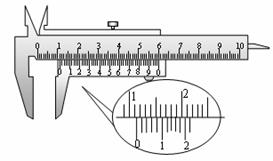
22.(17分)(1)用游标为50分度的卡尺,测定某圆筒的内径时,卡尺上的示数如图,可读出圆筒的内径为________mm。
(2)在液体中下落的物体最终会达到一个恒定的速度,称之为收尾速度。一个半径为 的球体在液体中下落的收尾速度为
的球体在液体中下落的收尾速度为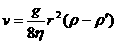 ,其中
,其中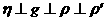 分别为液体的粘滞系数(与液体种类相关的常数)、重力加速度(本题中为已知量)、球体的密度、液体的密度。某同学为了测定某已知密度的液体的粘滞系数,选定了下列器材:一只1000mL的量筒、一块秒表、一把刻度尺、直径不同的铝球若干个(最大直径约10.00mm)。
分别为液体的粘滞系数(与液体种类相关的常数)、重力加速度(本题中为已知量)、球体的密度、液体的密度。某同学为了测定某已知密度的液体的粘滞系数,选定了下列器材:一只1000mL的量筒、一块秒表、一把刻度尺、直径不同的铝球若干个(最大直径约10.00mm)。
①请列出该同学漏选的器材: 。
②实验时,该同学首先将直径约10.00mm的铝球重复从装满被测液体的量筒面上自由落下测定它通过量筒刻度线750mL到500mL和450mL到200mL的两段时间,列表如下:
|
距离L(mL) |
时间t(s) |
平均时间t’(s) |
|
750-500 |
1.74 1.72 1.72 |
1.73 |
|
450-200 |
1.73 1.72 1.73 |
1.73 |
由以上测量数据得到的结论是 。
③若测出了不同半径的铝球的收尾速度,并已知球体和液体的密度,要求出液体的粘滞系数,对以上数据应如何处理?
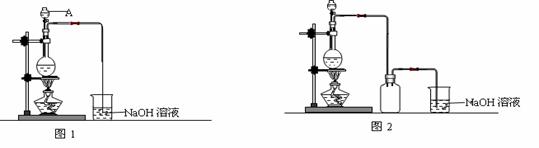
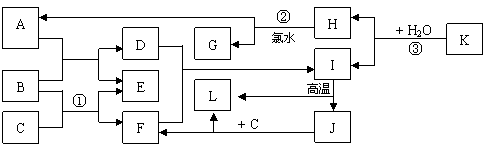
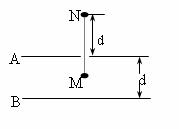 (2)油滴N所带电量的范围是多少?
(2)油滴N所带电量的范围是多少?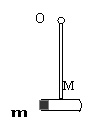 (1)乙醚要消耗多少内能;
(1)乙醚要消耗多少内能;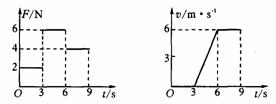
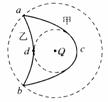 A.甲粒子经过c点时与乙粒子经过d点时具有相同的动能
A.甲粒子经过c点时与乙粒子经过d点时具有相同的动能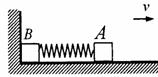 A.弹簧伸长量最大时的弹性势能等于弹簧压缩量最
A.弹簧伸长量最大时的弹性势能等于弹簧压缩量最