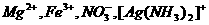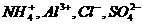 21.(15分)为了在实验室模拟用二氧化氮溶于水生成硝酸,现进行如下实验:
21.(15分)为了在实验室模拟用二氧化氮溶于水生成硝酸,现进行如下实验:
|
(1)实验室常用浓硝酸与铜反应制备二氧化氮,
化学方程式是 。
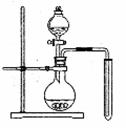
(2)可用右图装置制备并收集一试管二氧化氮,
①在加入药品前,必须进行的操作是
。
②该装置的缺点是(只填一个缺点既可)
 。
。
实验二:尽可能多地使试管中的二氧化氮被水吸收
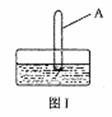
(3)将装有二氧化氮的试管A倒插入水中(图1),
并轻轻晃动试管,观察到的现象是:
反应的化学方程式是
(4)从下图中挑选所需的仪器,完成制取O2,并将O2通入到上述实验后的试管A中。
①画出制取O2装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置不用画),并表明所用试剂。
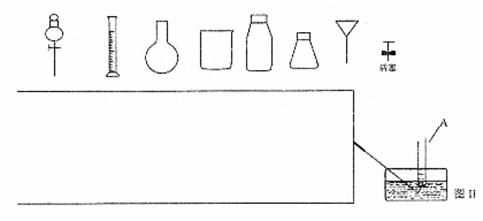
②某同学在图Ⅱ的试管A内通入O2的过程中没有观察到液面上升,而是试管内充满了无色气体,主要原因是 。
22.(15分)某化学研究性学习小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氧化铜并测定样品中氧化铜的质量分数,其实验流程图如下:
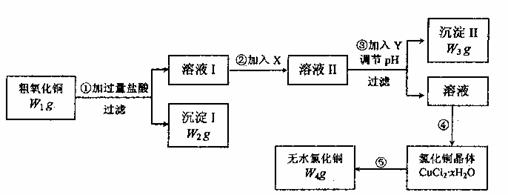
实验过程中的pH调节可参考下表:
|
物质 |
开始沉淀是的pH |
完全沉淀时的pH |
|
氢氧化铁 |
2.7 |
3.7 |
|
氢氧化亚铁 |
7.6 |
9.6 |
|
氢氧化铜 |
5.2 |
6.4 |
回答以下问题:
(1)步骤①过滤操作中所用仪器有铁架台(带铁圈)、漏斗、烧杯等,还需要使用的仪器用品有 。
(2)步骤①中发生的离子反应方程式 。
(3)步骤②溶液I中加入X的目的是 。
(4)试剂Y可选用(填字母) ,选择的原因是
。
a.氢氧化钠 b.氨水 c.碱式碳酸铜 d.氧化铜
(5)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·xH2O中其原因是
。
(6)经检测,CuCl2·xH2O中含水28.6%,则CuCl2·xH2O中x的值为 。
(7)看步骤④中有80%的氯化铜转入晶体,其余各步转化都是完全的,请根据流程图中表示的质量数据,写出样品中氧化铜的质量分数计算式 。
16.几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
L |
M |
X |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
A.离子半径大小:r(M+3)>r(T2-)
B.R的氧化物对应的水化物可能具有两性
C.X单质可在氧气燃烧生成XO3
D.L、X形成的简单离子核外电子数相等
15.下列反应离子方程式正确的是 ( )
A.Fe2(SO4)3的酸性溶液中通入足量硫化氢 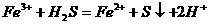
B.碳酸氢钙溶液中加入过量氢氧化钠溶液
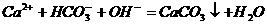
C.氯化铝溶液中加入过量氨水 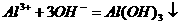
|