0 36302 36310 36316 36320 36326 36328 36332 36338 36340 36346 36352 36356 36358 36362 36368 36370 36376 36380 36382 36386 36388 36392 36394 36396 36397 36398 36400 36401 36402 36404 36406 36410 36412 36416 36418 36422 36428 36430 36436 36440 36442 36446 36452 36458 36460 36466 36470 36472 36478 36482 36488 36496 447348
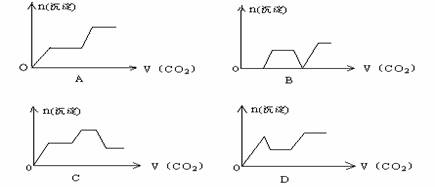
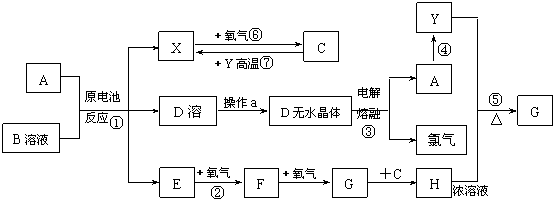 (10分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:
(10分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图: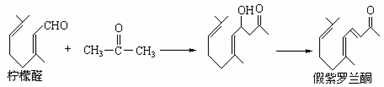 又知:R-X+H2O®R-OH+HX(“R-”为烃基)
下面是一种有机物A的合成路线,请回答有关问题:
又知:R-X+H2O®R-OH+HX(“R-”为烃基)
下面是一种有机物A的合成路线,请回答有关问题:
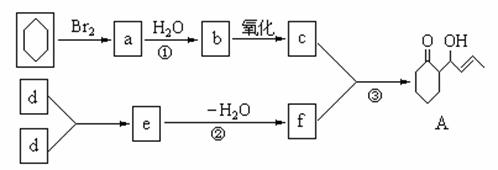
 ,煮沸去掉过量的Br2;
,煮沸去掉过量的Br2; (3)将右图所示的分液漏斗中下层液体放出的操作步骤为:
(3)将右图所示的分液漏斗中下层液体放出的操作步骤为: