24.(本小题共10分) 某工厂的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯。以上各物质的沸点如下:
|
物质 |
丙酮 |
乙酸乙酯 |
乙醇 |
乙酸 |
|
沸点/℃ |
56.2 |
77.06 |
78 |
117.9 |
现拟通过下列步骤回收乙醇和乙酸:①向废液中加入烧碱溶液,调整溶液的pH=10;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加热浓硫酸(过量),然后再放出耐酸蒸馏器中进行蒸馏,回收馏出物,请回答下列问题:
(l)加入烧碱使溶液的 pH=10的目的是________________________________
(2)在70℃~85℃时馏出物的主要成分为____________________________________。
(3)在步骤④中加入过量的浓硫酸的目的是(用化学方程式表示)
_______________________。
(4)最后蒸馏的温度控制在85℃~125℃之间,经过一段时间后,蒸馏瓶中残留液中溶质的主要成分是__________________________。
23.(本小题共9分) 利用右图装置,选用适当的试剂,可完成实验(1)、(2)、(3),并得出相应的结论。实验(l)、(2)、(3)所用试剂或所得结论列表如下。请完善表格,填写表中的空白处(填写所用试剂或实验结论):
|
实验 |
所用试剂 |
实验结论 |
||
|
甲 |
乙 |
丙 |
||
|
(1) |
① |
KMnO4 |
② |
氧化性MnO4一> Cl2>Br2 |
|
(2) |
盐酸 |
石灰石 |
苯酚钠 |
③ |
|
(3) |
④ |
⑤ |
⑥ |
证明还原性S2->Br- |
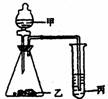 (1) ①________________________,②___________________________;
(1) ①________________________,②___________________________;
(2) ③____________________________________________________
(3) ④___________________,_________________,_______________。
20. (本小题共9分)实验室为了制得少量
漂白粉,常用浓盐酸与二氧化锰先制
C12,再用 Cl2与消石灰反应。已知 Cl2
与 Ca(OH)2制漂白粉是放热反应,
温度稍高即会发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有甲、乙、
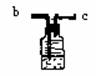
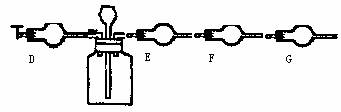
丙三套装置(U形管中放有玻璃纤维,可使气体顺利通过。)
(1)请对三套装置的优缺点进行评价,将以下的适当选项序号填于下表内。
A.容易引起环境污染 B.可防止环境污染 C. 可防止副反应发生
D.易发生副反应 e. 易控制反应速率 f.不易控制反应速率
|
|
优点 |
缺点 |
|
甲 |
|
|
|
乙 |
|
|
|
丙 |
|
|
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G)组装一套你认为更完善的实验装置,则连接顺序为(按气流从左到右方向):______________。

 (1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后 D. 实验过程中胶头滴管放置桌上
D. 实验过程中胶头滴管放置桌上