9.a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下: (98上海)
|
粒子代码 |
a |
b |
c |
d |
e |
f |
g |
|
原子核数 |
单核 |
单核 |
双核 |
多核 |
单核 |
多核 |
多核 |
|
带电荷数(单位电荷) |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可形成两个共价型g分子。
试写出:(1)a粒子的核外电子排布式
(2) b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为 > (用化学式表示)
(3) d溶于水的电离方程式
(4) g粒子所构成的晶体类型属
(5) c粒子是 ,f粒子是 (用化学式表示)
(1)1s22S22p6 (2)NaOH>Mg(OH)2 `(3) NH3+H2O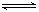 NH3·H2O
NH3·H2O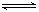 NH
NH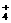 +OH- (4)分子晶体
+OH- (4)分子晶体
 =90,也可以由欧拉定律计算键数(即棱边数):60+(12+20)-2 = 90,C60分子所含单键数为:C60分子中单键为:90-30=60。(答“2×30(双键数)=60”即给2分) (4) 设C70分子中五边形数为x,六边形为y。依题意可得方程组:
=90,也可以由欧拉定律计算键数(即棱边数):60+(12+20)-2 = 90,C60分子所含单键数为:C60分子中单键为:90-30=60。(答“2×30(双键数)=60”即给2分) (4) 设C70分子中五边形数为x,六边形为y。依题意可得方程组: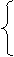
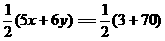 (键数,即棱边数)
(键数,即棱边数) (欧拉定理)
(欧拉定理)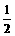 =90个。又由于90个价键中有
=90个。又由于90个价键中有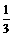 的价键为双键,
的价键为双键,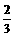 为单健,故分子中双键数为30个,单健数为60个。
为单健,故分子中双键数为30个,单健数为60个。 60+(x+y)-2=60×3×
60+(x+y)-2=60×3×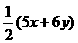 =60×3×
=60×3×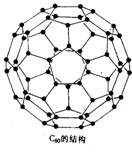

 )3
)3  =
=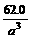 g·cm-3
g·cm-3
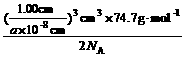 同样给分)
同样给分) =6.20×10-23
g
=6.20×10-23
g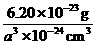 =
=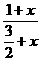 =
=
