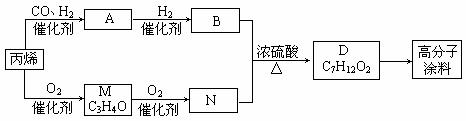
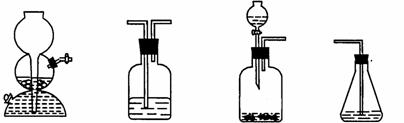
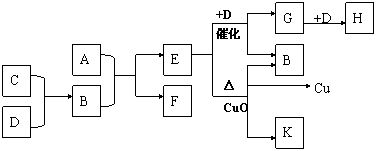26.(13分)某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成。称取天然碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如下表:
|
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
盐酸液的体积(mL) |
30 |
30 |
30 |
30 |
|
样品(g) |
3.32 |
4.15 |
5.81 |
7.47 |
|
二氧化碳的体积(mL) |
672 |
840 |
896 |
672 |
(1)由第Ⅰ组数据中的CO2体积与样品质量之比,可以推测用2.49g样品进行同样的实验时,产生CO2_________mL(标准状况)。
(2)另取3.32g天然碱样品于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式。
(3)已知Na2CO3和HCl(aq)的反应分下列两步进行:
Na2CO3+HCl = NaCl+NaHCO3
NaHCO3+HCl = NaCl+CO2↑+H2O
由上表中第Ⅳ组数据可以确定所用的HCl(aq)的浓度为 mol·L-1
(4)依据上表所列数据以及天然碱的化学式,讨论并确定上述实验中CO2(标准状况)体积V(mL)与样品质量W(g)之间的关系式。
19.(6分)有两瓶失去标签的白色固体,一瓶是KCl,一瓶是(NH4)2SO4。请你设计两种实验方案加以鉴别,简要写出操作过程、实验现象和结论。
|
方案 |
操作过程(简要叙述) |
现象和结论 |
|
(1) |
|
|
|
(2) |
|
|