21、(10分)硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g) 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度 |
450 |
500 |
550 |
600 |
|
SO2的转化率% |
97.5 |
95.8 |
90.50 |
80.0 |
(1)由表中数据判断△H 0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是
A. 容器的压强不变 B. 混合气体的密度不变
C. 混合气体中SO3的浓度不变 D. C(SO2)=C(SO3)
E.V正(SO2)=V正(SO3) F. V正(SO3)=2V逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1.
①0~2min之间,O2的反应速率为 .
②此时的温度为 ℃.
③此温度下的平衡常数为 (可用分数表示).

 (4)若将平衡反应混合物的压强增大(假如体积可变),平衡将
向移动.
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将
向移动.
18、(7分)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
⑴盛装0.2000 mol/L盐酸标准液应该用 式滴定管。
⑵滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_____________。直到因加入一滴盐酸后,溶液由黄色变为橙色,并______________________________为止。
⑶ 滴定操作可分解为如下几步:
①检查滴定管是否漏水; ②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤用蒸馏水洗涤玻璃仪器 ⑥滴定操作
正确的操作顺序为: 。
⑷有关数据记录如下:
|
实验序号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
|
|
滴定前 |
滴定后 |
||
|
1 |
20.00 |
0.50 |
20.70 |
|
2 |
20.00 |
6.00 |
26.00 |
|
3 |
20.00 |
1.40 |
21.20 |
则NaOH溶液的物质的量浓度为______________mol/L。
⑸若只用蒸馏水冲洗锥形瓶,则测定结果_________________;若滴定前平视读数,滴定终点时俯视读数,则会使所测酸的浓度值 。(填“无影响”、“偏高”或“偏低”)。
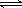 HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6)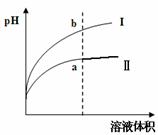
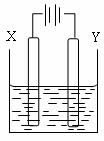 ②到燃料电池消耗2.8L O2(标准状况下)时,计算此时NaCl溶液的pH= (假设溶液的体积不变,气体全部从溶液中逸出)。在Y极通过的电子的物质的量为: 。
②到燃料电池消耗2.8L O2(标准状况下)时,计算此时NaCl溶液的pH= (假设溶液的体积不变,气体全部从溶液中逸出)。在Y极通过的电子的物质的量为: 。  对于可逆反应A(g)+2B(g)
对于可逆反应A(g)+2B(g)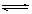 2C(g) △H>0,下列图象中正确的是( )
2C(g) △H>0,下列图象中正确的是( )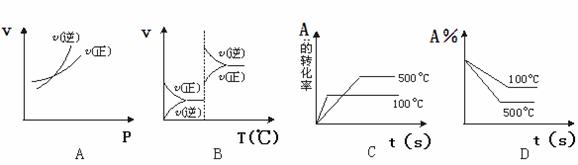
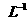 氨水中的Ksp比在20mL 0.01mol·
氨水中的Ksp比在20mL 0.01mol·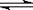 H+
+ OH-。下列叙述中,正确的是 ( )
H+
+ OH-。下列叙述中,正确的是 ( )