摘要:硫酸工业中SO2转化为SO3是重要的反应之一.在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)2SO3(g).SO2的转化率随温度的变化如下表所示: 温度 450 500 550 600 SO2的转化率% 97.5 95.8 90.50 80.0 (1)由表中数据判断△H 0 (2)能判断该反应是否达到平衡状态的是 A. 容器的压强不变 B. 混合气体的密度不变 C. 混合气体中SO3的浓度不变 D. C(SO2)=C(SO3) E.V正(SO2)=V正(SO3) F. V正(SO3)=2V逆(O2) (3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1. ①0~2min之间.O2的反应速率为 . ②此时的温度为 ℃. ③此温度下的平衡常数为 . (4)若将平衡反应混合物的压强增大.平衡将 向移动.
网址:http://m.1010jiajiao.com/timu3_id_320560[举报]
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)
2SO3(g),SO2的转化率随温度的变化如下表所示:
(1)由表中数据判断△H
(2)能判断该反应是否达到平衡状态的是
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为
②此时的温度为
③此温度下的平衡常数为
(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将
查看习题详情和答案>>
| 催化剂 |
| 加热 |
| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
<
<
0(填“>”、“=”或“<”)(2)能判断该反应是否达到平衡状态的是
ACF
ACF
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为
0.08mol?L-1?min-1
0.08mol?L-1?min-1
.②此时的温度为
600
600
℃.③此温度下的平衡常数为
| 400 |
| 21 |
| 400 |
| 21 |
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将
正
正
向移动.硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)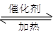 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度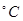 | 450 | 475 | 500 | 525 | 550 | 575 | 600 | 650 |
| SO2的转化率% | 97.5 | 95.8 | 95.8 | 93.5 | 90.50 | 85.6 | 80.0 | 73.7 |
(2)能判断该反应是否达到平衡状态的是
A. 容器的压强不变 B. 混合气体的密度不变
C. 混合气体中SO3的浓度不变 D. C(SO2)=C(SO3)
E. v正(SO2)=v正(SO3) F. v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1.
①0~2min之间,O2的反应速率为 .
②此时的温度为
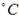 .③此温度下的平衡常数为 (可用分数表示).
.③此温度下的平衡常数为 (可用分数表示).④若将平衡反应混合物的压强增大1倍(假如体积可变),此时Qc为 ,平衡将 向移动。 查看习题详情和答案>>
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)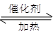 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
|
温度 |
450 |
475 |
500 |
525 |
550 |
575 |
600 |
650 |
|
SO2的转化率% |
97.5 |
95.8 |
95.8 |
93.5 |
90.50 |
85.6 |
80.0 |
73.7 |
(1)由表中数据判断△H 0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是
A. 容器的压强不变 B. 混合气体的密度不变
C. 混合气体中SO3的浓度不变 D. C(SO2)=C(SO3)
E. v正(SO2)=v正(SO3) F. v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1.
①0~2min之间,O2的反应速率为 .
②此时的温度为  .③此温度下的平衡常数为 (可用分数表示).
.③此温度下的平衡常数为 (可用分数表示).
④若将平衡反应混合物的压强增大1倍(假如体积可变),此时Qc为 ,平衡将 向移动。
查看习题详情和答案>>
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)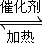 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
(1)由表中数据判断△H______0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
查看习题详情和答案>>
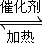 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3) F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
查看习题详情和答案>>
硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)
2SO3(g),SO2的转化率随温度的变化如下表所示:
(1)由表中数据判断△H______0(填“>”、“=”或“<”)
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变B.混合气体的密度不变
C.混合气体中SO3的浓度不变D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3)F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
查看习题详情和答案>>
| 催化剂 |
| 加热 |
| 温度°C | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(2)能判断该反应是否达到平衡状态的是______
A.容器的压强不变B.混合气体的密度不变
C.混合气体中SO3的浓度不变D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3)F.v正(SO3)=2v逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol?L-1.
①0~2min之间,O2的反应速率为______.
②此时的温度为______℃.
③此温度下的平衡常数为______(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将______向移动.
