0 31407 31415 31421 31425 31431 31433 31437 31443 31445 31451 31457 31461 31463 31467 31473 31475 31481 31485 31487 31491 31493 31497 31499 31501 31502 31503 31505 31506 31507 31509 31511 31515 31517 31521 31523 31527 31533 31535 31541 31545 31547 31551 31557 31563 31565 31571 31575 31577 31583 31587 31593 31601 447348
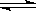 3C(气)
3C(气)
 pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:
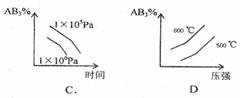
pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态: 对于可逆反应2AB3(g) A2(g)+3B2(g)(正反应吸热);下列图象正确的是
对于可逆反应2AB3(g) A2(g)+3B2(g)(正反应吸热);下列图象正确的是