25.(12分)
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
⑴准确称量8.2g含有少量中性易容杂质的样品,配成500ml待测溶液。称量时样品可放在 称量。
A.小烧杯中 B.洁净纸片上 C. 托盘上
⑵滴定过程中眼睛应注视 ;在铁架台上掂一张白纸,其目的是
⑶根据下表数据,计算被测烧碱样品的纯度是 。
|
滴定次数 |
待测溶液的体积(ml) |
标准盐酸(0.2000mol/L)体积 |
|
|
滴定前的刻度(ml) |
滴定后的刻度(ml) |
||
|
第一次 |
10.00 |
0.40 |
20.50 |
|
第二次 |
10.00 |
4.10 |
24.00 |
⑷下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
① 观察酸式滴定管液面时,开始时俯视,滴定终点平视,则滴定结果
② 若将锥形瓶用待测液润洗,然后再加入10.00ml待测液,则滴定结果
林口县第四中学2010-2011学年度上学期期中考试
24.(8分)
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO 2CO2+N2
2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间(s) K^S*5U.C#O% |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)(mol/L) |
1.00×10-3 |
4.50×10-4 |
2.50×10-4 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)(mol/L) |
3.60×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)= 。
(3)在该温度下,反应的平衡常数K= 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
22.(10分)
在100℃时,将0.200 mol的四氧化二氮气体充入2L真空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下表格:
|
时间 |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4) |
0.100 |
c1 |
0.050 |
c3 |
a |
b |
|
c(NO2) |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为_________________________________,达到平衡时四氧化二氮的转化率为________。
(2)20s时四氧化二氮的浓度c1=________mol·L-1,在0-20s时间段内,四氧化二氮的平均反应速率为________mol×L-1×s-1。
(3)若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为________mol•L-1。
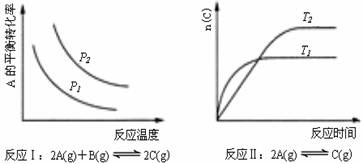

 B(g) + 3C(g)
△H<0,
B(g) + 3C(g)
△H<0,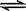
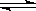 2Z(g) 不能说明该反应已达到平衡的标志是 ( )
2Z(g) 不能说明该反应已达到平衡的标志是 ( )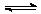 zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白: