7、下表中是各组反应的反应物和温度,反应刚开始时,放出H2速率最快的是( )
|
编号 金属(粉末状) 酸的浓度及体积
反应温度 (mol) (℃) |
|
A
Mg,0.1
6 mol·L-1 硝酸10mL
80 B Mg,0.1 3 mol·L-1 盐酸10mL 60 C Fe,0.1 3 mol·L-1L 盐酸10mL 60 D Mg,0.1 3 mol·L-1 硫酸10mL 60 |
14、(14分)将3 mol A和2.5 mol B混合于2L的密闭容器中,发生反应的化学方程式为:
3A(气) + B(气)  xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 试计算:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 试计算:
(1)x = A 的平均反应速率 (2) 平衡时C的浓度
(3) 平衡时B的转化率
(4) 平衡时,容器内的压强与原容器内压强的比值
高二 化学科答题纸
选择题
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
非选择题
|
11(11分) (1) (2)① ② 12.(15分) (1) (2) 13.(18分) (1)K= K值 (2) (3) (4) (5) 14(14分) (1)x= (2) (3) (4) |
 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动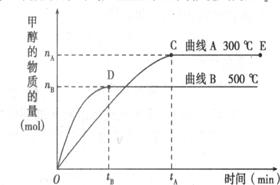 根据题意完成下列各题:
根据题意完成下列各题: CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是: