18.(12分). X是由两种元素组成的化合物,常温下呈液态,D、H、I是三种单质,其中H、I是常见金属,D是气体,G是一种红棕色固体。有关物质的转化关系如下图,图中省去了某些反应条件及部分生成物。
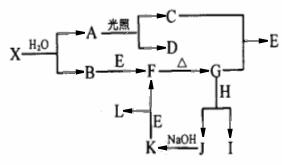 试回答下列问题:
试回答下列问题:
(1)写出G的化学式 ;
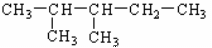
A的结构式 。
(2)已知X中两种元素的质量比为 28:213,
则X与水反应的化学方程式 。
(3) 简述检验E的阳离子的方法 。
(4) 写出下列反应的方程式
①写出G+H → J+I反应的化学方程式 。
②写出K+E → L+F的离子方程式 。



 w.w.w.k.s.5.u.c.o
w.w.w.k.s.5.u.c.o
19(10分)在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为:
5C2O42-+2MnO4-+16H+==10CO2↑+2Mn2++8H2O
以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol·L-1的高锰酸钾溶液500 mL。
步骤二:准确称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配高锰酸钾溶液进行滴定。三次平行实验的数据记录在下表中:
|
平行实验编号 |
Na2C2O4质量 (m g) |
滴定管起始读数(mL) |
滴定管滴定终点读数(mL) |
|
1 |
1.34 |
0.00 |
25.02 |
|
2 |
1.34 |
0.02 |
25.00 |
|
3 |
1.34 |
0.18 |
25.18 |
试回答下列问题:
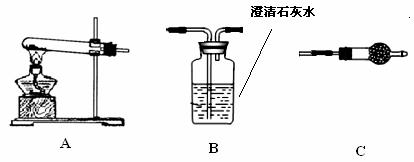
(1步骤一中要用到的主要玻璃仪器除烧杯外需 。
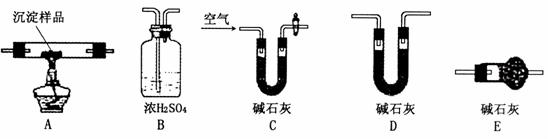
(2)步骤二中滴定操作图示正确的是 (填编号)。
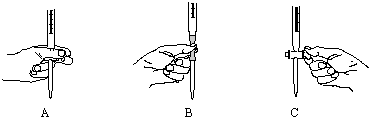
(3)步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是 。
(4)从实验所得数据计算,KMnO4溶液的浓度为 mol·L-1。
(5)如果在滴定过程中滴定管漏液,则测定结果将 (填“偏高”、“偏低”或“无影响”下同),滴定结束后俯视读数,则测定结果将 。
 B.
B. C.
C.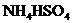 D.
D.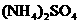
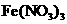 B.
B.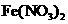
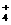 、K+、CO
、K+、CO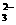 、SO
、SO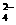 等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:
等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示: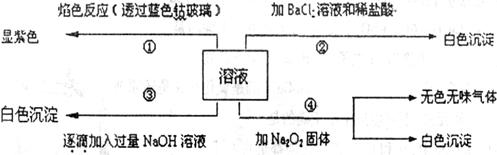

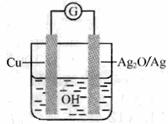 D. 电池工作时,溶液中 OH-向正极移动
D. 电池工作时,溶液中 OH-向正极移动