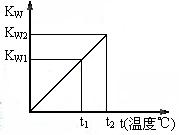
17.水的离子积常数KW与温度t(℃)的关系如右图所示:
(1)若t1=25℃,则KW1=_______;若t2=100℃时,KW2=
10-12,则0.05mol·L-1的Ba(OH)2溶液的pH=_______。
(2)已知25℃时,0.1L0.1mol·L-1的NaA溶液的pH=10,则
NaA溶液中所存在的化学平衡有(用离子方程式表示):
______________。溶液中各离子的物质的量浓度由大到小的顺序为________________。
(3)25℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为___________。
(4)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强碱的pH(pH酸)与强碱的pH(pH碱)之间应满足的关系为:
pH(酸)+pH(碱)=_______________。
溶液的酸碱性、pH 值及计算
重点回顾:
⒈定义:PH= ,广泛pH的范围为0-14。
注意:当溶液中[H+]或[OH-]大于1mol/L时,不用pH表示溶液的酸碱性。
⒉溶液的酸碱性:
溶液的酸碱性 常温(25℃)
中性溶液:C(H+) C(OH-) C(H+) 1×10- 7mol/L pH 7
酸性溶液:C(H+) C(OH-) C(H+) 1×10-7mol/L pH 7
碱性溶液:C(H+) C(OH-) C(H+) 1×10-7mol/L pH 7
⒊溶液PH的测定方法
(1)酸碱指示剂法
说明:常用的酸碱指示剂有石蕊、甲基橙、酚酞试液。
常用酸碱指示剂的pH变色范围
|
指示剂 |
变色范围的pH |
||
|
石蕊 |
<5 色 |
5-8 色 |
>8 色 |
|
甲基橙 |
<3.1 色 |
3.1-4.4 色 |
>4.4 色 |
|
酚酞 |
<8 色 |
8-10 色 |
>10 色 |
(2)pH试纸法
使用方法:
(3)PH计法
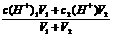
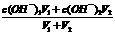
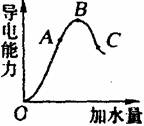 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答:
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答: