27].(9分)铝是国民经济发展的重要材料,铝在地壳中含量约占8%,目前我国铝消费超过430万吨,在众多的金属中仅次于钢铁。试完成(1)、(2)两小题
(1)实验室中用金属铝制备少量氢氧化铝,有以下3种方案
方案1:Al→Al3+→Al(OH)3
方案2:Al→AlO2-→Al(OH)3
|
方案3: |
Al→Al2(SO4)3 |
 →Al(OH)3 →Al(OH)3 |
|
Al→NaAlO2 |
制备相同物质的量的氢氧化铝消耗酸和碱最少的方案是 ;按最优方案,每制备1molAl(OH)3,至少消耗3mol/LH2SO4溶液 mL,6mol/LNaOH溶液 mL。
(2)工业上制取铝的流程图如下:
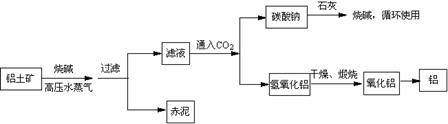
在制取氧化铝中,分析铝土矿和赤泥所得数据如下:
|
|
Al2O3 |
Fe2O3 |
NaOH |
其它杂质 |
|
铝土矿 |
55% |
16% |
0 |
/ |
|
赤泥 |
15% |
48% |
8% |
/ |
设杂质不参加反应,则每生产a吨纯净氧化铝,需铝土矿多少吨?投入的烧碱固体多少吨?
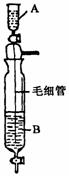 [21].(5分)在Inorganic
Syntheses一书中,有一装置是用以制备某种干燥的纯净气体,如下图所示:其A中应盛放一种密度比B中密度小的液体。下表中为几种液体的密度
[21].(5分)在Inorganic
Syntheses一书中,有一装置是用以制备某种干燥的纯净气体,如下图所示:其A中应盛放一种密度比B中密度小的液体。下表中为几种液体的密度
|
溶液名称 |
浓盐酸 |
浓硫酸 |
浓氨水 |
浓氢氧化钠溶液 |
浓醋酸 |
|
密度(g/mL) |
1.19 |
1.84 |
0.89 |
1.41 |
1.06 |
现从上述液体中选出几种适宜的试剂来利用该装置制出干燥纯净气体.
(1)制备出的气体其化学式是 。(写出全部可以制备的气体)
(2)应选用的试剂:A中盛 ;B中盛 。(任写一组)
(3)装置中毛细管的作用是 。
22].(12分)二氯化硫(SCl2)熔点-78℃,沸点59℃。密度1.638。遇水易分解。SCl2与SO3作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是由氯气与硫反应合成二氯化硫的实验装置。
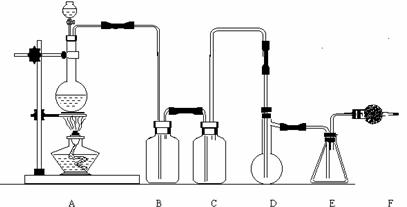
(1)装置A中发生反应的化学方程式为 。
(2)装置B盛放的药品是 ;C中是 。
(3)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是 。
(4)实验时,D装置需加热至50-59℃,最好采用何种方式 加热。如何防止E中液体挥发 。
(5)F装置中干燥管内所盛物质是 ,作用是 。
(6)二氯化硫电子式为 ;由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为 。
(7)亚硫酰极易水解,也能与乙醇等有机试剂反应,写出上述反应方程式 。
 [5].慈溪中学某研究性学习小组在施老师指导下做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色。判断下列说法中正确的是
[5].慈溪中学某研究性学习小组在施老师指导下做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色。判断下列说法中正确的是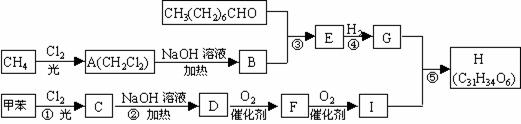
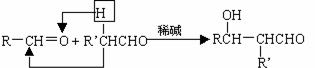
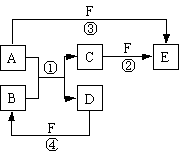 [23].(10分)A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件未标出),其中反应①是置换反应。
[23].(10分)A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件未标出),其中反应①是置换反应。