摘要:4].硫酸铜遇到黄铁矿(FeS2)可以发生反应:CuSO4+FeS2+H2O - Cu2S+FeSO4+H2SO4.在该反应中.被氧化的硫原子与被还原的硫原子的物质的量之比为 A 7︰3 B 3︰7 C 7︰5 D 5︰7 [5].慈溪中学某研究性学习小组在施老师指导下做了一个如图所示的实验.发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液.溶液显红色.判断下列说法中正确的是 A 该条件下生成的水分子化学性质比较活泼 B 该条件下H2被冷却为液态氢.液氢的水溶液具有还原性 C 该条件下H2燃烧生成了具有还原性的物质 D 该条件下H2燃烧的产物中可能含有一定量的H2O2
网址:http://m.1010jiajiao.com/timu3_id_263970[举报]
硫酸铜遇到黄铁矿(FeS2)可以发生反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,在该反应中,被氧化的硫原子与被还原的硫原子的物质的量之比为:
- A.7∶3
- B.3∶7
- C.7∶5
- D.5∶7
硫酸铜遇到黄铁矿(FeS2)可以发生反应: 14CuSO4 + 5FeS2 + 12H2O = 7Cu2S + 5FeSO4 + 12H2SO4 ,在该反应中,被氧化的硫原子与被还原的硫原子的物质的量之比为: ( )
A. 7:3 B. 3:7 C. 7:5 D. 5:7
查看习题详情和答案>>|
硫酸铜遇到黄铁矿(FeS2)可以发生反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,在该反应中,被氧化的硫原子与被还原的硫原子的物质的量之比为: | |
| [ ] | |
A. |
7∶3 |
B. |
3∶7 |
C. |
7∶5 |
D. |
5∶7 |
以下是某学习小组对乙二酸的某些性质进行研究性学习的过程:
【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
又知:
①草酸在100℃时开始升华,157℃时大量升华,并开始分解.
②草酸钙不溶于水.
③草酸蒸气能使澄清石灰水变浑浊.
④草酸蒸气在低温下可冷凝为固体.
根据上述材料提供的信息,回答下列问题:
【提出猜想】
(猜想一)根据草酸晶体的组成对其分解产物进行猜想
设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,请用下列装置组成一套探究实验装置(草酸晶体分解装置略,装置可重复使用,连接导管略去).
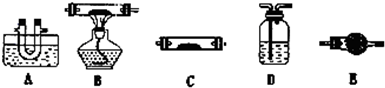
A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰
请回答下列问题:
①装置的连接顺序为:A→ .
②检验产物中CO的实验现象是 .
③整套装置是否存在不合理之处, (填是或否),若有该如何解决
.
(猜想二)乙二酸具有弱酸性
设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是 (填字母).
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性
设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性.配平该反应的离子方程式:
MnO4-+ H2C2O4+ H+═ Mn2++ CO2↑+ H2O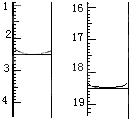
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4?2H2O及其它一些杂质)中H2C2O4?2H2O的含量.
方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol?L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4?2H2O的质量分数为 .(已知相对原子质量:Mr(H2C2O4?2H2O)=126)
查看习题详情和答案>>
【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4?2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | - |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g?cm-3) | 1.900 | 1.650 |
①草酸在100℃时开始升华,157℃时大量升华,并开始分解.
②草酸钙不溶于水.
③草酸蒸气能使澄清石灰水变浑浊.
④草酸蒸气在低温下可冷凝为固体.
根据上述材料提供的信息,回答下列问题:
【提出猜想】
(猜想一)根据草酸晶体的组成对其分解产物进行猜想
设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,请用下列装置组成一套探究实验装置(草酸晶体分解装置略,装置可重复使用,连接导管略去).

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰
请回答下列问题:
①装置的连接顺序为:A→
②检验产物中CO的实验现象是
③整套装置是否存在不合理之处,
(猜想二)乙二酸具有弱酸性
设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性
设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性.配平该反应的离子方程式:

(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4?2H2O及其它一些杂质)中H2C2O4?2H2O的含量.
方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol?L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4?2H2O的质量分数为
硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其与石灰乳混合可得“波尔多液”.实验室里需用180mL 0.10mol?L-1的硫酸铜溶液,则应选用的容量瓶规格和称取溶质的质量分别为( )
| A、180mL容量瓶,称取2.88g硫酸铜 | B、200mL容量瓶,称取5.00g胆矾 | C、250mL容量瓶,称取6.25g胆矾 | D、250mL容量瓶,称取4.0g硫酸铜 |