22.(6分)根据已有内容的规律进行增补
(1)同族元素单质间的置换反应的化学方程式:
①2Na+2H2O=2NaOH+H2↑ ②2HBr+Cl2=2HCl+Br2
③2H2S+O2=2S+2H2O ④
(2)已知
|
化学键 |
Si-O |
Si-Cl |
H-Cl |
Si-Si |
|
键能/KJ·mol-1 |
460 |
360 |
431 |
176 |
回答下列问题:
①比较熔点SiCl4 SiO2(填“>”或“<” ),
②工业制纯硅反应:1/2SiCl4(g)+H2(g)=1/2Si(s)+2HCl(g)△H=+118KJ·mol-1
则H-H键能为 KJ·mol-1
21.(10分)下图是元素周期表的短周期部分,序号a-h代表8种常见元素。
|
|
IA |
|
O族 |
|||||||
|
第一周期 |
a |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
|
||
|
第二周期 |
|
|
|
b |
c |
d |
|
|
||
|
第三周期 |
e |
|
f |
|
|
g |
h |
|
||
请用相应的化学用语回答下列问题:
(1)画出g原子结构示意图 。
(2)写出元素h的单质与元素a、c形成的简单化合物发生置换反应的化学方程式
。
(3)写出f单质与a、d、e三种元素形成的化合物水溶液反应的化学方程式
。
(4)a、b元素形成的最简单化合物与d单质可组成燃料电池(以KOH溶液作电解质溶
液),写出正极的电极反应式: ,负极发生 反
应(填“氧化”或“还原”),OH-移向 极。
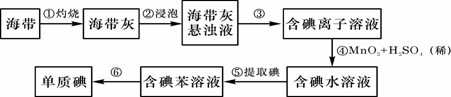
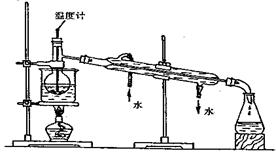 装置中的错误之处。
装置中的错误之处。