26、(12分)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
|
实验 编号 |
温度 (℃) |
大理石 规格 |
HNO3浓度(mol/L) |
实验目的 |
|
① |
25 |
粗颗粒 |
2.00 |
(I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究 对反应速率的影响 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
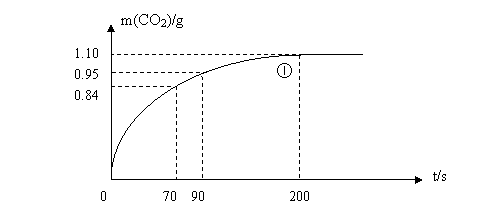
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70s-90s
范围内用HNO3表示的平均反应速率 (忽略溶液体积的变化)
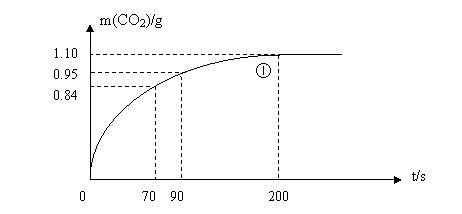

(3)请在上图中画出实验②③④中CO2质量随时间变化的关系的预期结果示意图。
|
 牡一中2009-2010学年下学期期中考试
牡一中2009-2010学年下学期期中考试
高一学年化学科1套卷 答题卡( 共100 分)
22、几种短周期元素的主要化合价及原子半径数据见下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
主要化合价 |
+2 |
+3 |
+6
-2 |
+7
-1 |
-2 |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.074 |
据表中信息判断,下列有关叙述中正确的是( ) A.L、M的单质分别与同浓度的稀盐酸反应时,M的单质反应更剧烈 B.M与T形成的化合物能和强酸、强碱反应 C.L与R两元素形成的化合物中含有共价键 D.Q、T两元素的氢化物热稳定性比较:Q的氢化物大于T的氢化物