19.关于化学键的叙述正确的是( )
| A. | 离子化合物中只存在离子键 | |
| B. | 非金属元素组成的化合物中可能存在离子键 | |
| C. | 由不同种元素组成的多原子分子里,一定只存在极性共价键 | |
| D. | 含金属元素的化合物中一定存在离子键 |
18.下列说法正确的是( )
| A. | 随原子序数递增,ⅦA族元素的最高价氧化物对应水化物酸性逐渐增强 | |
| B. | 第三周期元素中(除稀有气体元素)简单离子半径最小的元素,其氧化物具有两性 | |
| C. | 第三周期气态氢化物的沸点均为同主族中沸点最低的,是因为其分子内含有氢键 | |
| D. | 第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |
17.设NA为阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 1molCaC2中含有阴离子数目为2NA | |
| B. | 向FeI2溶液中通入氯气,当有2molFe2+被氧化时,转移电子的数目为2NA | |
| C. | 2.8g乙烯与丙烯的混合物中含碳原子的数目为0.4NA | |
| D. | 用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移电子数目为8NA |
15.下列说法不正确的是( )
| A. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| B. | 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理 | |
| C. | 某光学检测技术具有极高的灵敏度,可检测到单个细胞(V=10-12L)内的数个目标分子,据此可推算该检测技术能测量到细胞内浓度约为10-12~10-11mol•L-1的目标分子 | |
| D. | 油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应 |
13.设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个N2分子和NA个CO2原子个数比为1:1 | |
| B. | 1 mol H2O的质量与NA个H2O质量的总和几乎相等 | |
| C. | 1mol H2所含的原子数为NA | |
| D. | 1mol H2SO4中所含的粒子数目一定是NA |
12.下列实验操作中正确的是( )
| A. | 分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球插入蒸馏烧瓶中液体的液面以下 | |
| C. | 可用酒精萃取碘水中的碘 | |
| D. | 称量时,称量物放在托盘天平的右盘,砝码放在托盘天平的左盘 |
11.实验过程中下列操作正确的是( )
| A. | 给盛有2/3体积液体的试管加热 | |
| B. | CuSO4溶于水,可将含有CuSO4的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 实验时将剩余的钠放回原试剂瓶 |
10.除去粗盐中的不溶性固体可用过滤的方法,该操作中不需要用到的仪器是( )
0 172556 172564 172570 172574 172580 172582 172586 172592 172594 172600 172606 172610 172612 172616 172622 172624 172630 172634 172636 172640 172642 172646 172648 172650 172651 172652 172654 172655 172656 172658 172660 172664 172666 172670 172672 172676 172682 172684 172690 172694 172696 172700 172706 172712 172714 172720 172724 172726 172732 172736 172742 172750 203614
| A. | 蒸发皿 | B. | 玻璃棒 | C. | 烧杯 | D. | 漏斗 |
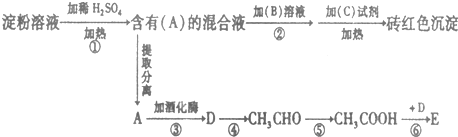
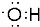 ;
;