17.已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D单质在C单质中燃烧时剧烈放热并发出耀眼的白光,A、B形成的气态化合物的水溶液呈碱性.下列说法错误的是( )
| A. | 原子半径:D>E>B>C>A | |
| B. | 热稳定性:EA4<A2C | |
| C. | B元素的最高价氧化物的水化物与D单质反应不能生成A2气体 | |
| D. | 化合物DC与化合物EC2中化学键类型相同 |
16.下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
| A. | 半导体材料碳化硅 | B. | 超导材料铜锌合金 | ||
| C. | 透明陶瓷材料硒化锌 | D. | 超导材料Cs3C60 |
15.下列说法正确的是( )
| A. | 由非金属元素形成的化合物都是共价化合物 | |
| B. | 酸、碱发生反应,只要生成1mol水放出的热量就相同 | |
| C. | 原电池工作时电流从正极流向负极 | |
| D. | 某物质溶于水得到的溶液可以导电,则该物质一定是离子化合物 |
14.三种气态烃混合物VmL和足量氧气混合后,经点燃爆炸并恢复到原状况,体积共缩小2VmL,若所有气体体积均在25℃,101kPa下测定,则三种烃的组合不可能是( )
| A. | CH4 C2H4 C3H4 | B. | CH4 C2H6 C2H2 | C. | C2H2 C2H4 C3H4 | D. | C2H2C3H6 C4H8 |
13.将乙醛和乙酸分离的正确方法是( )
| A. | 加热蒸馏 | |
| B. | 利用银镜反应进行分离 | |
| C. | 加入Na2CO3后,通过萃取的方法分离 | |
| D. | 先加入烧碱溶液,之后蒸馏出乙醛;再加入浓硫酸,蒸馏出乙酸 |
12.下列装置所示的实验中,能达到实验目的是( )
| A. |  分离碘和酒精 | B. | 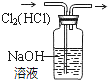 除去CL2中HCL | C. | 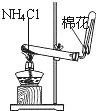 实验室制氨气 | D. | 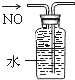 排水法收集NO |
11.利用原料气在合成塔中合成NH3,为加快正反应速率,且提高N2的转化率所采取的措施是( )
| A. | 加压 | B. | 移走氨气 | C. | 使用催化剂 | D. | 充入N2 |
10.将浓硫酸和稀硫酸在实验室中分别敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )

| A. | a挥发、b吸水 | B. | a升华、b冷凝 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
9.黑火药爆炸时可发生如下反应:5S+16KNO3+16C=3K2SO4+4K2CO3+K2S+12CO2↑+8N2↑,下列有关说法正确的是( )
| A. | S既作氧化剂又作还原剂 | B. | 消耗12gC时,反应转移5mol电子 | ||
| C. | 还原产物只有K2S | D. | KNO3只发生氧化反应 |
8.下列解释实验事实的离子方程式正确的是( )
0 170977 170985 170991 170995 171001 171003 171007 171013 171015 171021 171027 171031 171033 171037 171043 171045 171051 171055 171057 171061 171063 171067 171069 171071 171072 171073 171075 171076 171077 171079 171081 171085 171087 171091 171093 171097 171103 171105 171111 171115 171117 171121 171127 171133 171135 171141 171145 171147 171153 171157 171163 171171 203614
| A. | 纯碱溶液显碱性的原因:CO32-+2H2O?H2CO3+2OH- | |
| B. | 氯化铁溶液腐蚀铜线路板Cu+Fe3+=Cu2++Fe2+ | |
| C. | 稀硫酸与氢氧化钡溶液恰好中和:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 氯气溶于水:Cl2+H2O=H++Cl-+HClO |