题目内容
15.下列说法正确的是( )| A. | 由非金属元素形成的化合物都是共价化合物 | |
| B. | 酸、碱发生反应,只要生成1mol水放出的热量就相同 | |
| C. | 原电池工作时电流从正极流向负极 | |
| D. | 某物质溶于水得到的溶液可以导电,则该物质一定是离子化合物 |
分析 A、氯化铵由非金属元素形成的化合物,是离子化合物;
B、根据中和热的概念分析;
C、原电池工作时电子从负极流向正极,电流方向相反;
D、二氧化碳溶于的水溶液导电.
解答 解:A、氯化铵由非金属元素形成的化合物,是离子化合物,故A错误;
B、中和热是在稀溶液中强酸与强碱发生中和反应生成1mol水时所释放的热量,这时放出的热量才相等,弱酸弱碱电离要吸热,而浓酸浓碱溶解要发热,故B错误;
C、原电池工作时电子从负极流向正极,电流方向相反,所以电流从正极流向负极,故C正确;
D、二氧化碳溶于的水溶液导电,但二氧化碳是非电解质,故D错误;故选C.
点评 本题考查学生化学键、原电池的反应原理和反应热和焓变之间的关系知识,注意知识的归纳和应用是关键,难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
6.在常温下,将一定体积的某 NaOH 溶液分成两等分,与pH均为2的一元酸 HA、HB恰好中和,消耗两种酸溶液的体积分别为V1、V2(V1≠V2).则下列叙述中正确的是( )
| A. | 若 Vl>V2,则说明HA的酸性比 HB的酸性强 | |
| B. | 中和后得到的两种溶液的pH均为 7 | |
| C. | 分别将两种酸溶液稀释10 倍后溶液的pH均为3 | |
| D. | 分别往等体积的两种酸溶液中加人足量锌粉,充分反应后产生的H2的体积相等 |
10.将浓硫酸和稀硫酸在实验室中分别敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )

| A. | a挥发、b吸水 | B. | a升华、b冷凝 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
4.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 88g乙酸乙酯中存在的共价键总数为14NA | |
| C. | 加热时,含2molH2SO4的浓硫酸与足量铜反应,转移的电子数为2NA | |
| D. | 1mol羟基所含的电子数为10NA |
13.活性氧化锌是一种多功能的新型无机材料,某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如图:
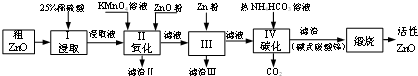
已知各相关氢氧化物沉淀pH范围如下表所示:
完成下列填空:
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要D(选填编号)
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤Ⅱ中通过加入KMnO4的作用是MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O(用离子方程式表示);
(3)用ZnO调节pH,可以除去含铁杂质.检验Fe3+是否沉淀完全的实验操作是取少量溶液,滴加KSCN溶液,无颜色变化,说明沉淀完全,反应沉淀不完全,调节pH的适宜范围是4.1~4.7;
(4)步骤Ⅲ中加入Zn粉的作用是:①除去溶液中的Cu2+;②进一步调节溶液pH;
(5)步骤IV中使用热NH4HCO3溶液能促进Zn2+转化为沉淀,但温度不宜过高,其原因可能是NH4HCO3分解导致损失.
(6)用如下方法测定所得活性氧化锌的纯度:
①取1.000g活性氧化锌,用15.00mL 1.000mol/L硫酸溶液完全溶解,滴入几滴甲基橙,
②用浓度为0.500mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL.
判断滴定终点的方法是溶液颜色由红色变为黄色,且半分钟不变色,所得活性氧化锌的纯度为97.2%;
(7)已知常温下,CuS的溶度积常数Ksp=6.0×10-36,物质的量浓度为3.0×10-3mol•L-1Na2S溶液与等体积的CuSO4溶液中混合后立即产生沉淀,则CuSO4的浓度最小为4.0×10-33mol•L-1.

已知各相关氢氧化物沉淀pH范围如下表所示:
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要D(选填编号)
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤Ⅱ中通过加入KMnO4的作用是MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O(用离子方程式表示);
(3)用ZnO调节pH,可以除去含铁杂质.检验Fe3+是否沉淀完全的实验操作是取少量溶液,滴加KSCN溶液,无颜色变化,说明沉淀完全,反应沉淀不完全,调节pH的适宜范围是4.1~4.7;
(4)步骤Ⅲ中加入Zn粉的作用是:①除去溶液中的Cu2+;②进一步调节溶液pH;
(5)步骤IV中使用热NH4HCO3溶液能促进Zn2+转化为沉淀,但温度不宜过高,其原因可能是NH4HCO3分解导致损失.
(6)用如下方法测定所得活性氧化锌的纯度:
①取1.000g活性氧化锌,用15.00mL 1.000mol/L硫酸溶液完全溶解,滴入几滴甲基橙,
②用浓度为0.500mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL.
判断滴定终点的方法是溶液颜色由红色变为黄色,且半分钟不变色,所得活性氧化锌的纯度为97.2%;
(7)已知常温下,CuS的溶度积常数Ksp=6.0×10-36,物质的量浓度为3.0×10-3mol•L-1Na2S溶液与等体积的CuSO4溶液中混合后立即产生沉淀,则CuSO4的浓度最小为4.0×10-33mol•L-1.
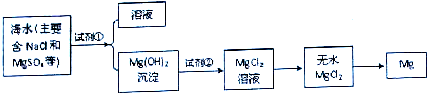
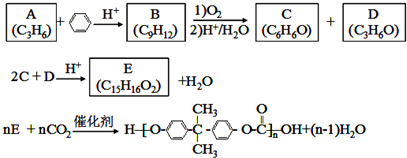
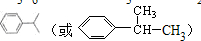 ;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚.
;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$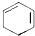 +2NaBr+2H2O.
+2NaBr+2H2O.