题目内容
12.下列装置所示的实验中,能达到实验目的是( )| A. |  分离碘和酒精 | B. | 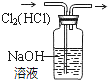 除去CL2中HCL | C. | 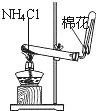 实验室制氨气 | D. | 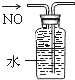 排水法收集NO |
分析 A.分液分离能分层的物质;
B.氯气、HCl均能与NaOH溶液反应;
C.氨气与氯化氢反应生成氯化铵;
D.一氧化氮不溶于水不与水反应.
解答 解:A.碘和酒精互溶,不分层,不能用分液分离,故A错误;
B.氯气、HCl均能与NaOH溶液反应,则不能利用碱来除去氯气中的HCl,故B错误;
C.氨气与氯化氢反应生成氯化铵,得不到氨气,故C错误;
D.一氧化氮不溶于水不与水反应,可用排水法收集,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质制备及分离与提纯、气体收集等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
3.在一定条件下,某化合物W受热分解:2W$\frac{\underline{\;△\;}}{\;}$A↑+2B↑+4C↑,测得反应后生成的混合气体是相同条件下等体积H2质量的11.43倍,则W的摩尔质量是( )
| A. | 11.43 | B. | 22.86g/mol | C. | 80.01 | D. | 80.01g/mol |
20.已知1mol氢气完全燃烧生成水蒸气时放出热量242kJ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol H-H键断裂时吸收热量为( )
| A. | 920 kJ | B. | 557 kJ | C. | 436 kJ | D. | 188 kJ |
17.已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D单质在C单质中燃烧时剧烈放热并发出耀眼的白光,A、B形成的气态化合物的水溶液呈碱性.下列说法错误的是( )
| A. | 原子半径:D>E>B>C>A | |
| B. | 热稳定性:EA4<A2C | |
| C. | B元素的最高价氧化物的水化物与D单质反应不能生成A2气体 | |
| D. | 化合物DC与化合物EC2中化学键类型相同 |
4. 锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,下列叙述正确的是( )
锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,下列叙述正确的是( )
 锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,下列叙述正确的是( )
锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,下列叙述正确的是( )| A. | 锰原子核内有25个质子,一个锰原子的质量是54.94g | |
| B. | 锰原子核外有4个电子层,其化学性质由最内层电子决定 | |
| C. | MnO2属于氧化物,在H2O2分解制O2的实验中做催化剂 | |
| D. | KMnO4为紫黑色固体,易溶于水、汽油等溶剂,形成紫红色溶液 |
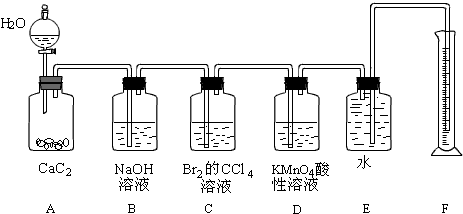
 ;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用饱和食盐水来代替水.
;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用饱和食盐水来代替水.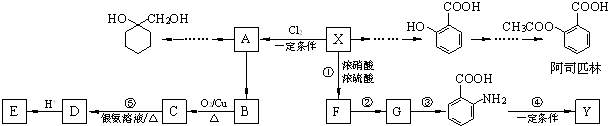
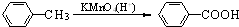
 (苯胺,易被氧化)
(苯胺,易被氧化)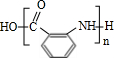 .
. 有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式:
有多种同分异构体,写出同时符合下列4个条件它的同分异构体的结构简式: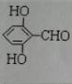 、
、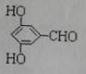 .
.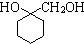 的流程图:
的流程图:
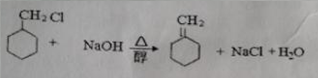 .
.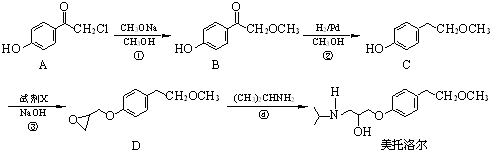
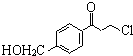 为原料
为原料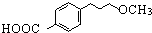 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).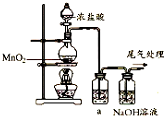 某兴趣小组的同学用如图装置制取漂白液(有效成分为NaClO),并研究其相关性质.
某兴趣小组的同学用如图装置制取漂白液(有效成分为NaClO),并研究其相关性质.