20.关于物质的分离、除杂方法不正确的是( )
| A. | 通过萃取、分液将乙醇和水分离 | |
| B. | 通过蒸馏将海水淡化 | |
| C. | 通过加热除去固体碳酸钠中混有的碳酸氢钠 | |
| D. | 通过溶解、过滤除去粗盐中的泥沙 |
19.关于吸热反应、放热反应的叙述正确的是( )
| A. | Ba(OH)2+H2SO4═BaSO4↓+2H2O既是放热反应又是氧化还原反应 | |
| B. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O反应物的总能量低于生成物的总能量 | |
| C. | C(石墨)$\frac{一定条件}{\;}$C(金刚石)是吸热反应,所以金刚石比石墨更稳定 | |
| D. | 吸热反应和放热反应都遵守能量守恒定律 |
18.如图所示装置,关于此装置的叙述不正确的是( )
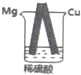

| A. | 是将化学能转化成电能的装置 | |
| B. | Cu上有气体放出 | |
| C. | Mg是负极,电极反应是Mg-2e-═Mg2+ | |
| D. | 导线中有电流通过,电流方向是由Mg到Cu |
17.在一定温度下的恒容密闭容器中,充入一定量的NO2,发生2NO2(g)?N2O4(g)反应,达到化学平衡状态的标志是( )
| A. | NO2或N2O4的浓度不再变化 | B. | c(NO2)=c(N2O4) | ||
| C. | v正(NO2)=v逆(N2O4) | D. | NO2、N2O4的总质量不再变化 |
16.利用金属活动性的不同,可以采用不同的冶炼方法.下面关于金属冶炼叙述正确的是( )
| A. | 高炉炼铁采用了热分解法 | |
| B. | 电解氯化钠溶液冶炼金属钠 | |
| C. | 依据Fe+CuSO4═FeSO4+Cu的原理冶炼金属铜 | |
| D. | 金属冶炼的实质是将金属元素从其化合物中氧化出来 |
15.下列组成和结构都相同的是( )
| A. | 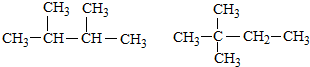 | |
| B. | 液氯、氯气 | |
| C. | O2、O3 | |
| D. | ${\;}_{17}^{35}Cl$、${\;}_{17}^{37}Cl$ |
14.能源与材料、信息被称为现代社会发展的三大支柱.下列相关叙述正确的是( )
| A. | 石油分馏能得到石油气、汽油和煤油等清洁能源 | |
| B. | 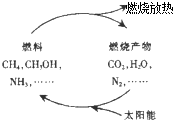 在如图循环转化过程中,太阳能最终转化为热能 | |
| C. | 煤的干馏是指将煤在空气中加热的过程,工业上也叫煤的焦化 | |
| D. | 糖类、油脂、蛋白质是为了人类生命活动提供能量的基本营养物质,都能发生水解反应 |
13.下列化学用语使用不正确的是( )
| A. | N2的结构式 N≡N | B. | 氯化铵的电子式 | C. | S2-的结构示意图 | D. | 甲烷的比例模型  |
12.绿色化学的核心就是利用化学原理从源头上减少和 消除工业生产对环境的污染.下列转化符合绿色化学原则,且原子利用率为100%的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH2Cl+HCl | B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | ||
| C. | CH2=CH2+Br2$\stackrel{一定条件}{→}$CH2BrCH2Br | D. | 3NO2+H2O═2HNO3+NO |
11.CuCl2常用于颜料、木材防腐等工业,并用作消毒剂、媒染剂、催化剂.工业上用粗制的氧化铜粉末(含杂质FeO和SiO2)来制取无水CuCl2的流程如下:

已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
(1)第②步反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-.
(2)滤渣A的成分有SiO2(填化学式),检验滤液C中的Fe3+离子是否除尽的方法是取滤液C少量于试管中,滴加几滴KSCN溶液,若溶液变为血红色,证明滤液C中的Fe3+离子未除尽,反之已除尽.
(3)第④步蒸发操作必要的仪器有铁架台(含铁圈)、坩埚钳、石棉网、酒精灯、蒸发皿、玻璃棒.需要在氯化氢气流中蒸干制取无水氯化铜的原因是HCl抑制CuCl2水解.
(4)称取30.250g已制得的无水CuCl2产品(含少量FeCl3杂质),溶于水中,加入过量的铁粉充分反应后过滤,得250mL滤液,量取25.00mL滤液于锥形瓶中,用0.100mol?L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积平均为46.00mL,则该无水CuCl2产品中CuCl2的质量分数为0.89(用小数表示,计算结果保留2位小数).
0 170653 170661 170667 170671 170677 170679 170683 170689 170691 170697 170703 170707 170709 170713 170719 170721 170727 170731 170733 170737 170739 170743 170745 170747 170748 170749 170751 170752 170753 170755 170757 170761 170763 170767 170769 170773 170779 170781 170787 170791 170793 170797 170803 170809 170811 170817 170821 170823 170829 170833 170839 170847 203614

已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
(2)滤渣A的成分有SiO2(填化学式),检验滤液C中的Fe3+离子是否除尽的方法是取滤液C少量于试管中,滴加几滴KSCN溶液,若溶液变为血红色,证明滤液C中的Fe3+离子未除尽,反之已除尽.
(3)第④步蒸发操作必要的仪器有铁架台(含铁圈)、坩埚钳、石棉网、酒精灯、蒸发皿、玻璃棒.需要在氯化氢气流中蒸干制取无水氯化铜的原因是HCl抑制CuCl2水解.
(4)称取30.250g已制得的无水CuCl2产品(含少量FeCl3杂质),溶于水中,加入过量的铁粉充分反应后过滤,得250mL滤液,量取25.00mL滤液于锥形瓶中,用0.100mol?L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积平均为46.00mL,则该无水CuCl2产品中CuCl2的质量分数为0.89(用小数表示,计算结果保留2位小数).