题目内容
18.如图所示装置,关于此装置的叙述不正确的是( )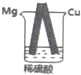
| A. | 是将化学能转化成电能的装置 | |
| B. | Cu上有气体放出 | |
| C. | Mg是负极,电极反应是Mg-2e-═Mg2+ | |
| D. | 导线中有电流通过,电流方向是由Mg到Cu |
分析 该装置中,镁易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析.
解答 解:A.镁易失电子作负极,铜作正极,形成原电池,将化学能转化成电能的装置,故A正确;
B.铜片上氢离子得电子生成氢气,所以Cu上有气体放出,故B正确;
C.镁易失电子作负极,电极反应是Mg-2e-═Mg2+,故C正确;
D.镁易失电子作负极,铜作正极,电流方向是由正极铜到负极镁,故D错误;
故选D.
点评 本题考查了原电池原理,明确正负极的判断方法、正负极发生的反应即可解答,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
1.下列实验装置能达到实验目的是(夹持仪器未画出)( )
| A. | 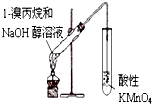 装置用于检验溴丙烷消去产物 | |
| B. | 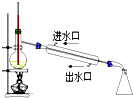 装置用于石油的分馏 | |
| C. | 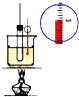 装置用于实验室制硝基苯 | |
| D. | 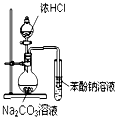 装置可装置证明酸性:盐酸>碳酸>苯酚 |
9.在中和滴定中,下列操作或说法不正确的是( )
| A. | 使用滴定管时,滴定管必须用待装液润洗2~3次 | |
| B. | 酸式滴定管不能盛装碱液,碱式滴定管不能盛装酸液或强氧化性溶液 | |
| C. | 盛装准确量取的待测液的锥形瓶应预先用待测液润洗 | |
| D. | 滴定终点时,若不慎滴入过量标准溶液,可用装有待测液的滴定管再滴入一定量进行调整 |
13.下列化学用语使用不正确的是( )
| A. | N2的结构式 N≡N | B. | 氯化铵的电子式 | C. | S2-的结构示意图 | D. | 甲烷的比例模型  |
3.0.1mol某烃完全燃烧后,能生成二氧化碳11.2L(标准状况下),此烃在一定条件下能与氢气加成,最多消耗氢气的物质的量是该烃的2倍,此烃的结构简式可能是( )
| A. | CH2=CH-CH3 | B. | CH2=CH-CH2-CH3 | ||
| C. | CH3=CH-CH2-CH=CH2 | D. | CH2=CH-CH2-CH2 |
7.下列物质中含有共价键的离子化合物是( )
①MgF2 ②NaClO ③NaOH ④NH4Cl ⑤CO2 ⑥N2.
①MgF2 ②NaClO ③NaOH ④NH4Cl ⑤CO2 ⑥N2.
| A. | ②③⑤ | B. | ②③④ | C. | ①②③ | D. | ①③⑤ |
8.下列说法不正确的是( )
石油$\stackrel{①}{→}$分馏产品$\stackrel{②}{→}$乙烯$\stackrel{③}{→}$CH2BrCH2Br.
石油$\stackrel{①}{→}$分馏产品$\stackrel{②}{→}$乙烯$\stackrel{③}{→}$CH2BrCH2Br.
| A. | 石油主要是由烃组成的混合物 | B. | ①主要发生物理变化 | ||
| C. | ②包括裂化,裂解等过程 | D. | ③中产物名称是二溴已烷 |

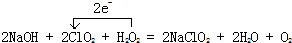 ;吸收装置中的温度不能过高,其原因是:防止H2O2的分解.
;吸收装置中的温度不能过高,其原因是:防止H2O2的分解. 某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.
某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.