题目内容
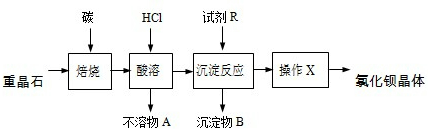
11.CuCl2常用于颜料、木材防腐等工业,并用作消毒剂、媒染剂、催化剂.工业上用粗制的氧化铜粉末(含杂质FeO和SiO2)来制取无水CuCl2的流程如下:
已知:Fe3+、Fe2+、Cu2+转化为相应的氢氧化物,开始沉淀和沉淀完全时的pH如下表:
| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
(2)滤渣A的成分有SiO2(填化学式),检验滤液C中的Fe3+离子是否除尽的方法是取滤液C少量于试管中,滴加几滴KSCN溶液,若溶液变为血红色,证明滤液C中的Fe3+离子未除尽,反之已除尽.
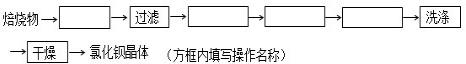
(3)第④步蒸发操作必要的仪器有铁架台(含铁圈)、坩埚钳、石棉网、酒精灯、蒸发皿、玻璃棒.需要在氯化氢气流中蒸干制取无水氯化铜的原因是HCl抑制CuCl2水解.
(4)称取30.250g已制得的无水CuCl2产品(含少量FeCl3杂质),溶于水中,加入过量的铁粉充分反应后过滤,得250mL滤液,量取25.00mL滤液于锥形瓶中,用0.100mol?L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积平均为46.00mL,则该无水CuCl2产品中CuCl2的质量分数为0.89(用小数表示,计算结果保留2位小数).
分析 粗制的氧化铜粉末(含FeO和SiO2杂质),加入盐酸,CuO+2HCl═CuCl2+H2O,FeO+2HCl═FeCl2+H2O,二氧化硅和盐酸不反应,滤渣A为SiO2,滤液A为:CuCl2、FeCl2,加氯水,氯气具有氧化性氧化亚铁离子2Fe2++Cl2=2Fe3++2Cl-,滤液B为:Fe3+、Cu2+、Cl-,加入氧化铜,氧化铜和氢离子反应,Fe3++3H2O?Fe(0H)3+3H+,调节PH至3.2,形成氢氧化铁沉淀,氯化铜水溶液中铜离子水解,在氯化氢气流中加热抑制氯化铜水解得到氯化铜固体,
(1)第②步加入氯水,氯气氧化亚铁离子;
(2)粗制的氧化铜粉末(含FeO和SiO2杂质),加入盐酸,氧化亚铁、氧化亚铜和酸反应生成易溶于水的盐,二氧化硅和酸不反应,难溶于水,Fe3+与硫氰化钾溶液反应,使溶液变红色,据此解答;
(3)根据蒸发操作所用的仪器分析判断,蒸发需要蒸发皿、酒精灯、玻璃棒等仪器;氯化铜水溶液中铜离子水解,在氯化氢气流中加热抑制氯化铜水解;
(4)Fe+2Fe3+=3Fe2+,铁和氯化铜反应Fe+Cu2+=Fe2++Cu生成氯化亚铁和铜,根据n=cV计算25mL样品溶液消耗高锰酸钾的物质的量,进而计算250mL溶液可以消耗高锰酸钾的物质的量,再根据5Fe2++MnO4-+8H+=5Fe3++2Mn2++4H2O离子方程式计算亚铁离子的物质的量,亚铁离子总量减去三价铁转化的铁离子可得由无水CuCl2转化的亚铁离子,根据铁守恒可得产品中CuCl2的物质的量,根据m=nM计算CuCl2的质量,进而计算其质量分数.
解答 解:粗制的氧化铜粉末(含FeO和SiO2杂质),加入盐酸,CuO+2HCl═CuCl2+H2O,FeO+2HCl═FeCl2+H2O,二氧化硅和盐酸不反应,滤渣A为SiO2,滤液A为:CuCl2、FeCl2,加氯水,氯气具有氧化性氧化亚铁离子2Fe2++Cl2=2Fe3++2Cl-,滤液B为:Fe3+、Cu2+、Cl-,加入氧化铜,氧化铜和氢离子反应,促进水解反应右移,Fe3++3H2O?Fe(0H)3+3H+,调节PH至3.2,形成氢氧化铁沉淀,氯化铜水溶液中铜离子水解,在氯化氢气流中加热抑制氯化铜水解得到氯化铜固体,
(1)氯气具有氧化性,亚铁离子具有还原性,第②步加入氯水,发生反应2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(2)粗制的氧化铜粉末(含FeO和SiO2杂质),加入盐酸,CuO+2HCl═CuCl2+H2O,FeO+2HCl═FeCl2+H2O,二氧化硅和盐酸不反应,CuCl2、FeCl2易溶于水,二氧化硅和酸不反应,难溶于水,所以滤渣A为SiO2,Fe3+与硫氰化钾溶液反应,使溶液变红色,所以检验滤液B中是否含Fe3+离子的方法为:取少量滤液C,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+,溶液不变红色,说明滤液中不含Fe3+,
故答案为:SiO2;取少量滤液C于试管中,向其中加入硫氰化钾溶液,溶液变血红色,证明滤液C中Fe3+未除尽,反之未除尽;
(3)蒸发时,需要使用蒸发皿;需要铁架台和铁圈支撑蒸发皿;需要玻璃棒进行搅拌,以防止液体受热不均匀,造成液体飞溅;需要酒精灯进行加热;坩埚钳用于夹持蒸发皿,滤液C是氯化铜溶液,制取无水CuCl2时,需在HCl气体中蒸干是防止氯化铜水解,HCl抑制CuCl2水解;
故答案为:酒精灯、蒸发皿、玻璃棒;HCl抑制CuCl2水解;
(4)称取30.250g已制得的无水CuCl2产品(含0.0204molFeCl3杂质),溶于水中,加入过量的铁粉,Fe+Cu2+=Fe2++Cu,Fe+2Fe3+=3Fe2+,用0.100mol•L-1酸性KMnO4溶液滴定5Fe2++MnO4-+8H+=5Fe3++2Mn2++4H2O,25mL样品溶液消耗高锰酸钾的物质的量为0.046L×0.100mol/L=4.6×10-3mol,可知250mL溶液可以消耗高锰酸钾的物质的量为4.6×10-3mol×$\frac{250mL}{25mL}$=4.6×10-2mol,由5Fe2++MnO4-+8H+=5Fe3++2Mn2++4H2O,可知250mL溶液中亚铁离子离子的物质的量为4.6×10-2mol×5=0.23mol,由Fe+2Fe3+=3Fe2+,三价铁转化的铁离子0.0204mol×$\frac{3}{2}$=0.0306mol,Fe+Cu2+=Fe2++Cu可得无水CuCl2产品中CuCl2的物质的量为0.23mol-0.0306mol=0.1994mol,故CuCl2的质量分数为$\frac{0.1994mol×135g/mol}{30.250g}$≈0.89,
故答案为:0.89.
点评 本题考查学生对元素及其化合物的主要性质的掌握、书写离子方程式、阅读题目获取新信息能力、对工艺流程的理解等,难度中等,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力,注意(4)滴定的计算.

| A. | 在c(HCO${\;}_{3}^{-}$)=0.1 mol•L-1的溶液中:NH${\;}_{4}^{+}$、Al3+、Cl-、NO${\;}_{3}^{-}$ | |
| B. | 有大量NO${\;}_{3}^{-}$存在的强酸性溶液中:NH${\;}_{4}^{+}$、Ba2+、Fe3+、Cl- | |
| C. | 由水电离出的c(H+)=1×10-12mol•L-1的溶液中:Na+、Al3+、CH3COO-、I- | |
| D. | 能使pH试纸变红的溶液中:ClO-、S2-、Na+、K+ |
| A. | 高炉炼铁采用了热分解法 | |
| B. | 电解氯化钠溶液冶炼金属钠 | |
| C. | 依据Fe+CuSO4═FeSO4+Cu的原理冶炼金属铜 | |
| D. | 金属冶炼的实质是将金属元素从其化合物中氧化出来 |
| A. | CH2=CH-CH3 | B. | CH2=CH-CH2-CH3 | ||
| C. | CH3=CH-CH2-CH=CH2 | D. | CH2=CH-CH2-CH2 |
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 用醋酸溶解石灰石:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO- | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| D. | Cu溶于稀硝酸:Cu+2H++NO3=Cu2++NO2↑+H2O |
| A. | 元素分析仪 | B. | 红外光谱仪 | C. | 质谱仪 | D. | 核磁共振仪 |


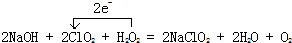 ;吸收装置中的温度不能过高,其原因是:防止H2O2的分解.
;吸收装置中的温度不能过高,其原因是:防止H2O2的分解.