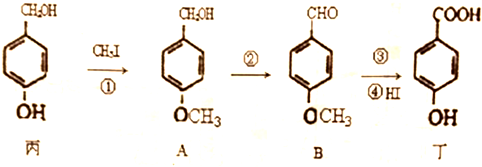
3.下列说法正确的是( )
| A. | 浓硫酸有吸水性,可用于干燥氨气 | |
| B. | SiO2是酸性氧化物,不与任何酸反应 | |
| C. | Na2O2与水反应、红热的Fe与水蒸气反应均能生成碱 | |
| D. | SO2通入少量紫色石蕊溶液,溶液始终呈红色 |
2.下列有关金属及其化合物的知识说法正确的是( )
| A. | 观察焰色反应实验为黄色火焰,则可证明该溶液中含有Na+ | |
| B. | 金属单质导电与电解质溶液导电原因是一样的 | |
| C. | 常温下浓硫酸与铜不反应,是因为铜遇浓硫酸发生了钝化反应 | |
| D. | 可用Na与MgCl2溶液反应制Mg |
1.现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)某同学根据上述信息,所画的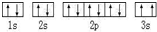 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.
(3)CD3中心原子的杂化方式为sp3,分子立体构型三角锥形形.
(4)E元素基态原子的电子占用15个原子轨道,有26种不同运动状态.
(5)F元素的元素符号为As,其基态原子的核外电子排布式1s22s22p63s23p63d104s24p3.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E元素的+3价离子有5个未成对电子 |
| F在周期表的第15列 |
(2)某同学根据上述信息,所画的
 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.(3)CD3中心原子的杂化方式为sp3,分子立体构型三角锥形形.
(4)E元素基态原子的电子占用15个原子轨道,有26种不同运动状态.
(5)F元素的元素符号为As,其基态原子的核外电子排布式1s22s22p63s23p63d104s24p3.
20.氯化硼(BCl3)的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp1杂化 | |
| C. | 氯化硼分子为共价化合物 | |
| D. | 氯化硼分子是极性分子 |
19.W、X、Y、Z是短周期元素,它们的核电荷数依次增大.下表列出它们的性质和结构:
(1)元素符号:XO,ZNa.
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式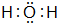 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
0 170513 170521 170527 170531 170537 170539 170543 170549 170551 170557 170563 170567 170569 170573 170579 170581 170587 170591 170593 170597 170599 170603 170605 170607 170608 170609 170611 170612 170613 170615 170617 170621 170623 170627 170629 170633 170639 170641 170647 170651 170653 170657 170663 170669 170671 170677 170681 170683 170689 170693 170699 170707 203614
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外S能级上的电子总数与P能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外P能级上的电子总数比S能级上的电子总数多2 |
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式
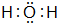 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.