题目内容
4.(1)在一个白色点滴板的二个孔穴中分别加入火柴梗、少量CuSO4•5H2O.分别滴入几滴浓硫酸,观察现象.回答下列问题:浓硫酸滴到火柴梗上,火柴梗变黑(填实验现象),说明浓硫酸具有脱水性.
浓硫酸滴入CuSO4•5H2O中,胆矾变白(填实验现象),说明浓硫酸具有吸水性.
(2)为探究Fe3+能转化为Fe2+,实验室提供下列试剂:铁粉、0.1mol•L-1 FeCl3溶液、0.1mol•L-1 FeCl2溶液、KSCN溶液、新制氯水.请你设计该实验方案(包括实验操作、实验现象及结论):取少量FeCl3溶液于试管中,加入足量铁粉,充分振荡后静置,滴加1至2滴KSCN溶液,无明显变化,说明Fe3+已转化为Fe2+.
分析 (1)浓硫酸使火柴梗变黑,是因其具有脱水性;滴入CuSO4•5H2O中变白,是因其具有吸水性;
(2)利用2FeCl3+Fe═3FeCl2,及亚铁离子遇KSCN溶液不变色来证明转化.
解答 解:(1)浓硫酸使火柴梗变黑,是因其具有脱水性,使火柴梗中的有机物中的H、O以水的形式脱出,只留下黑色的碳;滴入CuSO4•5H2O中变白,是因其具有吸水性,将晶体中的水吸收,故答案为:黑;脱水;变白;吸水;
(2)由2FeCl3+Fe═3FeCl2,及亚铁离子遇KSCN溶液不变色可知,取少量FeCl3溶液于试管中,加入足量的铁粉,反应后静置,滴加KSCN溶液,无现象,则说明Fe3+已转化为Fe2+,故答案为:取少量FeCl3溶液于试管中,加入足量铁粉,充分振荡后静置,滴加1至2滴KSCN溶液,无明显变化,说明Fe3+已转化为Fe2+.
点评 本题考查浓硫酸的性质及亚铁离子与铁离子的转化,侧重物质的性质及离子的性质的考查,注意亚铁离子遇KSCN溶液不变色,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
2.生活中碰到的某些问题常常涉及到化学知识,下列分析正确的是( )
| A. | 水在人体内没有调节体温的作用,但水是一种很好的溶剂 | |
| B. | 胃酸过多的人不宜吃海带、鸡肉、苹果等酸性食物 | |
| C. | 凡是有甜味的物质都是糖类,因此糖尿病人不能吃有甜味的食品 | |
| D. | 可用灼烧的方法来鉴别某白色纺织品的成分是真蚕丝还是“人造丝” |
15.下列物质能用化合反应直接制得的是( )
①FeCl2 ②Fe(OH)3 ③FeCl3 ④Fe(OH)2.
①FeCl2 ②Fe(OH)3 ③FeCl3 ④Fe(OH)2.
| A. | ①③ | B. | ①②③ | C. | ②③ | D. | ②④ |
19.W、X、Y、Z是短周期元素,它们的核电荷数依次增大.下表列出它们的性质和结构:
(1)元素符号:XO,ZNa.
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式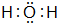 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外S能级上的电子总数与P能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外P能级上的电子总数比S能级上的电子总数多2 |
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式
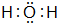 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
16.在同温同压下,下列各组热化学方程式中,△H2>△H 1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g),△H 1;2H2(g)+O2(g)=2H2O(l),△H2 | |
| B. | S(g)+O2(g)=SO2(g),△H 1;S(s)+O2(g)=SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g),△H 1;C(s)+O2(g)=CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g),△H 1;2H2(g)+2Cl2(g)=4HCl(g)△H2 |
13.某气态烃1mol和2mol氯化氢完全加成反应,所得产物还能和8molCl2发生取代反应,最后得到一种只含碳和氯两种元素的化合物,则原有气态烃可能为( )
| A. | CH≡CCH2CH2CH3 | B. | CH2CH2C≡CH | C. | CH2=CHCH3 | D. | CH≡CCH3 |
14.下列各溶液中,Na+的物质的量浓度最大的是( )
| A. | 4L 0.5mol•L-1的NaCl溶液 | B. | 1L 0.3mol•L-1的Na2SO4溶液 | ||
| C. | 0.8L 0.4mol•L-1的NaOH的溶液 | D. | 2L 0.15mol•L-1的Na3PO4的溶液 |
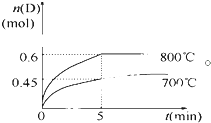 在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.