题目内容
7.下列物质中:①MgCl2 ②NaOH溶液 ③熔融KNO3 ④纯醋酸 ⑤Na ⑥氨气 ⑦乙醇⑧CaCO3 ⑨Al(OH)3 ⑩CO2
(1)属于强电解质的是:①③⑧;(填序号,以下同)
(2)属于非电解质的是:⑥⑦⑩.
分析 强电解质是在水溶液中或熔融状态下,能完全电离的电解质;包括强酸、强碱、活泼金属氧化物和大部分盐;
非电解质是指:在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子.
解答 解:①MgCl2溶于水和熔融状态下均能完全电离,属于强电解质;
②NaOH溶液属于混合物,既不是电解质也不是非电解质;
③熔融KNO3能导电,完全电离,属于强电解质;
④纯醋酸不能电离,溶于水完全电离,属于弱电解质;
⑤Na是金属单质,既不是电解质也不是非电解质;
⑥氨气不能导电,属于非电解质;
⑦乙醇溶于水和熔融状态下均不能导电,属于非电解质;
⑧CaCO3熔融状态下完全电离,属于强电解质;
⑨Al(OH)3为弱碱,属于弱电解质;
⑩CO2本身不能电离,溶于水后能生成的碳酸能电离,二氧化碳属于非电解质,故答案为:(1)①③⑧;(2)⑥⑦⑩.
点评 本题考查了强电解质与非电解质的定义,侧重考查学生的辨别能力,注意知识的归纳和整理是关键.

练习册系列答案
相关题目
5.我国卫生部门制定的《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”.香烟燃烧产生的烟气中,有多种有害物质,其中尼古丁对人体危害最大,尼古丁的分子式为C10H14N2. 下列说法正确的是( )
| A. | 尼古丁是由26个原子构成的物质 | |
| B. | 尼古丁中C、H、N三种元素的质量比为:10:14:2 | |
| C. | 尼古丁的相对分子质量是162g | |
| D. | 尼古丁中氮元素的质量分数为17.3% |
18. U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如右表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如右表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
(1)元素Z在周期表中位于VIIA族.我国首创以W组成的金属-海水-空气电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使W组成的金属不断氧化而产生电流.只要把灯放入海水中数分钟,就会发出耀眼的白光.则该电源负极反应为Al-3e-=Al3+.
(2)YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+,由此可知YO2和VO还原性较强的是(写化学式)SO2.
(3)V的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3+3H2O2=N2+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递增的是bc(填代号).
③温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为$\frac{4}{{a}^{2}}$.
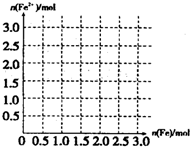
④向含4mol V的最高价含氧酸的稀溶液中,逐渐加入Fe粉至过量.假设生成的气体只有一种(VO),请在坐标系中画出n(Fe2+)随n(Fe)变化的示意图.
(4)相同温度下,等体积、物质的量浓度都为0.1mol/L的KZ和CH3COOK溶液的两种溶液中,离子总数相比较A.(填代号)
A.前者多 B.一样多C.后者多 D.无法判断.
 U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如右表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如右表;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.| U | ||
| Y |
(2)YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+,由此可知YO2和VO还原性较强的是(写化学式)SO2.
(3)V的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3+3H2O2=N2+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递增的是bc(填代号).
| 选项 | a | b | c | d |
| X | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |
④向含4mol V的最高价含氧酸的稀溶液中,逐渐加入Fe粉至过量.假设生成的气体只有一种(VO),请在坐标系中画出n(Fe2+)随n(Fe)变化的示意图.
(4)相同温度下,等体积、物质的量浓度都为0.1mol/L的KZ和CH3COOK溶液的两种溶液中,离子总数相比较A.(填代号)
A.前者多 B.一样多C.后者多 D.无法判断.
2.下列有关金属及其化合物的知识说法正确的是( )
| A. | 观察焰色反应实验为黄色火焰,则可证明该溶液中含有Na+ | |
| B. | 金属单质导电与电解质溶液导电原因是一样的 | |
| C. | 常温下浓硫酸与铜不反应,是因为铜遇浓硫酸发生了钝化反应 | |
| D. | 可用Na与MgCl2溶液反应制Mg |
12.既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的乙烯,得到较纯净的甲烷的方法是( )
| A. | 与足量溴水反应 | B. | 通入酸性高锰酸钾溶液中 | ||
| C. | 在一定条件下通入氢气 | D. | 将其分别点燃 |
19.下列叙述正确的是( )
| A. | 100℃纯水的c(H+)>10-7 mol/L,说明加热可导致水显酸性 | |
| B. | c(H+)=10-3 mol/L的醋酸溶液,稀释至10倍后c(H+)=10-4mol/L | |
| C. | 0.2mol/L的盐酸与等体积水混合后c(H+)=0.1 mol/L | |
| D. | 室温时,pH=3的盐酸和pH=11的氨水等体积混合,溶液显中性 |
16.25℃、101KPa时,2mol氢气燃烧生成水蒸气放出484KJ热量,下列热化学方程式正确的是( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-484kJ/mol | B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=+242kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-484kJ/mol |
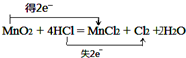 :
: