16.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
(1)请完成以下实验设计表(表中不要留空格):
(2)编号①实验测得容器中压强随时间变化如图2甲.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,请在图2乙中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式是O2+2H2O+4e-=4OH-.

(3)该小组对图2甲中0-t1时压强变大的原因提出了如下假设,请你完成假设二::
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案,请你再设计一个实验方案验证假设一.
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 0.5 | 2.0 | 36.0 | |
| ③ | 碳粉质量的影响 | 0.2 | 90.0 |

(3)该小组对图2甲中0-t1时压强变大的原因提出了如下假设,请你完成假设二::
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案,请你再设计一个实验方案验证假设一.
15.电解NO制备NH4NO3,其工作原理如图所示.下列说法不正确的是( )


| A. | 甲电极为阴极 | |
| B. | 为使电解产物全部转化为NH4NO3,需补充的物质为NH3 | |
| C. | 乙电极的电极反应式是:NO-3e-+4OH-=NO3-+2H2O | |
| D. | 该反应中NO既是氧化剂又是还原剂 |
14.下列说法正确的是( )
| A. | 任何一个氧化还原反应都可以设计为原电池,输出电能 | |
| B. | 常温下,将pH=2的盐酸和pH=12的氨水等体积混合后溶液呈碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| C. | 任何可逆反应,其平衡常数越大,反应速率、反应物的转化率越大 | |
| D. | pH=9的CH3COONa溶液和pH=9的NH3•H2O溶液,两溶液中水的电离程度相同 |
13.2SO2(g)+O2(g)$\frac{\underline{\;V_{2}O_{5}\;}}{\;}$2SO3(g)△H<0是制备硫酸的重要反应.下列关于该反应的叙述不正确的是( )
| A. | 降低温度将缩短反应达到平衡的时间 | |
| B. | 增大反应体系的压强反应速率一定增大 | |
| C. | 催化剂V2O5同时改变正逆反应速率 | |
| D. | 增加O2的浓度将提高SO2的转化率 |
12.在相同的温度下,100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
| A. | c(H+) | B. | 醋酸电离的程度 | ||
| C. | 中和时所需 NaOH的量 | D. | 醋酸的物质的量 |
11.下列说法正确的是( )
| A. | 电解MgCl2饱和溶液可制得金属镁 | |
| B. | 用浓硫酸与铁反应能增大生成H2的速率 | |
| C. | 电解饱和食盐水的过程中,水的电离平衡正向移动 | |
| D. | 纯银器在空气中露置其表面因电化学腐蚀渐渐变暗 |
10.下列做法能改善空气质量的是( )
0 169751 169759 169765 169769 169775 169777 169781 169787 169789 169795 169801 169805 169807 169811 169817 169819 169825 169829 169831 169835 169837 169841 169843 169845 169846 169847 169849 169850 169851 169853 169855 169859 169861 169865 169867 169871 169877 169879 169885 169889 169891 169895 169901 169907 169909 169915 169919 169921 169927 169931 169937 169945 203614
| A. | 限制使用电动车 | |
| B. | 利用太阳能、风能和氢能等能源代替化石燃料 | |
| C. | 鼓励私人购买和使用汽车代替公交车 | |
| D. | 以煤等燃料作为主要生活燃料 |
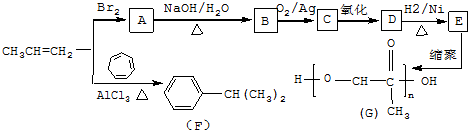
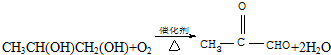 ,C发生银镜反应的化学方程式
,C发生银镜反应的化学方程式 .
.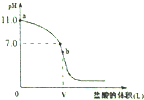 常温时,向浓度为0.1mol/L体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而变化的滴定曲线如图所示,b点表示两种溶液恰好完全反应.
常温时,向浓度为0.1mol/L体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而变化的滴定曲线如图所示,b点表示两种溶液恰好完全反应.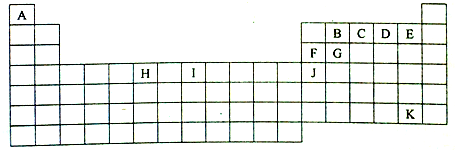
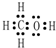 ,Y的中心原子杂化方式为SP2.
,Y的中心原子杂化方式为SP2.