18.太阳能的开发和利用是21世纪一个重要课题.利用储能介质储存太阳能的原理是:白天在太阳照射下某种盐熔化,吸收热量,晚间熔盐固化释放出相应的能量,已知数据:
其中最适宜选用作为储能介质的是( )
| 盐 | 熔点(℃) | 熔化吸热(kJ•mol-1) | 参考价格(元•t-1) |
| CaCl2•6H2O | 29.9 | 37.3 | 780~850 |
| Na2SO4•10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4•12H2O | 35.1 | 100.1 | 1 600~2 000 |
| Na2S2O3•5H2O | 45.0 | 49.7 | 1 400~1 800 |
| A. | CaCl2•6H2O | B. | Na2SO4•10H2O | C. | Na2HPO4•12H2O | D. | Na2S2O3•5H2O |
17.可逆反应:2NO(g)+O2(g)═2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
| A. | 单位时间内生成n mol O2的同时生成n mol NO2 | |
| B. | 混合气体的颜色不再改变的状态 | |
| C. | ν(NO2):ν(NO):ν(O2)=2:2:1的状态 | |
| D. | 混合气体的密度不再改变的状态 |
16.某烃的一种同分异构体的一氯代物只有一种,该烃的分子式是( )
| A. | C6H14 | B. | C5H12 | C. | C4H10 | D. | C3H8 |
15.元素在元素周期表中的位置可以反映元素的原子结构和性质,下列说法正确的是( )
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期中同主族元素的最外层电子数及化学性质完全相同 | |
| D. | 同周期元素的原子半径从左到右依次减小 |
13. Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
(1)若由0.2mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH>7,则混合溶液中各种离子浓度由大到小的顺序是:c(Na+)>c(A-)>c(OH-)>c(H+).
(2)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液pH<7的原因:等浓度时弱酸HA电离大于A-离子水解.
②两组溶液中c(A-)的大小,A组>B组(填“>”“<”或“=”);溶液中水的电离程度A组>B组(填“>”“<”或“=”).
(3)若HA为强酸,若是pH=2HA V1mL与pH=12Ba(OH)2 V2 mL混合后得到pH=11的溶液,则$\frac{{V}_{1}}{{V}_{2}}$=$\frac{9}{11}$
Ⅱ、现有浓度为0.1mol•L-1的五种电解质溶液①NaHSO4;②NaHCO3;③NaCl;④CH3COONa;⑤NaOH
(1)这五种溶液的pH由小到大的顺序是①<③<④<②<⑤(填编号).
(2)在上述五种溶液中分别加入Al2(SO4)3溶液,能产生大量无色无味气体的是②(填编号);其离子反应方程式为:3HCO3-+Al3+=Al(OH)3↓+3CO2↑.
Ⅲ.已知:
(1)在浓度均为0.01mol/L的CH3COONa、NaClO、Na2CO3的混合溶液中,逐滴加入0.01mol/L HCl,则体系中酸根离子反应的先后顺序为CO32-、ClO-、CH3COO-;(填酸根离子符号)
(2)25℃时,向20mL 0.1mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图象正确的是D.
 Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.(1)若由0.2mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH>7,则混合溶液中各种离子浓度由大到小的顺序是:c(Na+)>c(A-)>c(OH-)>c(H+).
(2)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液pH<7的原因:等浓度时弱酸HA电离大于A-离子水解.
②两组溶液中c(A-)的大小,A组>B组(填“>”“<”或“=”);溶液中水的电离程度A组>B组(填“>”“<”或“=”).
(3)若HA为强酸,若是pH=2HA V1mL与pH=12Ba(OH)2 V2 mL混合后得到pH=11的溶液,则$\frac{{V}_{1}}{{V}_{2}}$=$\frac{9}{11}$
Ⅱ、现有浓度为0.1mol•L-1的五种电解质溶液①NaHSO4;②NaHCO3;③NaCl;④CH3COONa;⑤NaOH
(1)这五种溶液的pH由小到大的顺序是①<③<④<②<⑤(填编号).
(2)在上述五种溶液中分别加入Al2(SO4)3溶液,能产生大量无色无味气体的是②(填编号);其离子反应方程式为:3HCO3-+Al3+=Al(OH)3↓+3CO2↑.
Ⅲ.已知:
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | HCN | 5×10-10 |
| H2CO3 | Ka1=4.2×10-7 | HClO | 3×10-8 |
| Ka2=5.6×10-11 |
(2)25℃时,向20mL 0.1mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图象正确的是D.
11.反应2SO2+O2?2SO3达到平衡后,再向反应容器中充入含氧的同位素的氧气,经过一段时间后,原子存在于( )
| A. | O2 | B. | SO2 | C. | O2和SO2 | D. | O2、SO2和SO3 |
10.现有一块生锈的铁片,在进行铁与Cu(NO3)2溶液的置换实验之前需要对铁片进行预处理,下列处理方式不可行的是( )
| A. | 用稀硝酸处理铁片 | B. | 用稀盐酸处理铁片 | ||
| C. | 用浓硝酸处理铁片 | D. | 用浓盐酸处理铁片 |
9.将铜粉放入稀H2SO4中,加热无明显现象,但加入某化合物后,发现铜粉质量逐渐减少,则该化合物不可能是( )
0 169508 169516 169522 169526 169532 169534 169538 169544 169546 169552 169558 169562 169564 169568 169574 169576 169582 169586 169588 169592 169594 169598 169600 169602 169603 169604 169606 169607 169608 169610 169612 169616 169618 169622 169624 169628 169634 169636 169642 169646 169648 169652 169658 169664 169666 169672 169676 169678 169684 169688 169694 169702 203614
| A. | Fe2(SO4)3 | B. | FeSO4 | C. | KNO3 | D. | Fe3O4 |
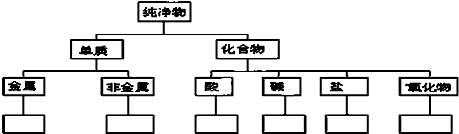
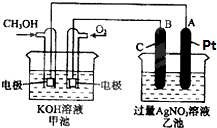 请按要求回答下列问题:
请按要求回答下列问题: