题目内容
10.现有一块生锈的铁片,在进行铁与Cu(NO3)2溶液的置换实验之前需要对铁片进行预处理,下列处理方式不可行的是( )| A. | 用稀硝酸处理铁片 | B. | 用稀盐酸处理铁片 | ||
| C. | 用浓硝酸处理铁片 | D. | 用浓盐酸处理铁片 |
分析 一块生锈的铁片,在进行铁与Cu(NO3)2溶液的置换实验之前需要对铁片进行预处理,即除去铁片表面的铁锈三氧化二铁,可以用酸清洗即可.
解答 解:一块生锈的铁片,在进行铁与Cu(NO3)2溶液的置换实验之前需要对铁片进行预处理,即除去铁片表面的铁锈三氧化二铁,可以用稀盐酸、稀硝酸、稀硫酸、浓盐酸等,但不能用浓硝酸,因为浓硝酸使铁发生钝化生成一层致密的氧化膜阻止与Cu(NO3)2溶液的置换,故选:C.
点评 本题主要考查了除去铁片表面的铁锈的方法,比较简单,注意浓硝酸和浓硫酸与铁发生钝化.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.用单分子油膜法测出油酸分子(视为球形)的直径后,还要下列哪一个物理量就可以计算出阿伏加德罗常数( )
| A. | 油滴的体积 | B. | 油滴的质量 | C. | 1 mol油酸的体积 | D. | 油酸的摩尔质量 |
8.某反应的化学方程式为:aFeCl2+bKNO3+cHCl═dFeCl3+eKCl+fX+gH2O,若b=1,d=3,则X的化学式为( )
| A. | N2 | B. | NO | C. | NO2 | D. | NH4Cl |
5.下列电子排布式中,原子处于激发态的是( )
| A. | 1s22s22p1 | B. | 1s22s22p33s1 | ||
| C. | 1s22s22p63s23p63d104s2 | D. | 1s22s22p63s23p63d34s2 |
15.元素在元素周期表中的位置可以反映元素的原子结构和性质,下列说法正确的是( )
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期中同主族元素的最外层电子数及化学性质完全相同 | |
| D. | 同周期元素的原子半径从左到右依次减小 |
2.下面的排序不正确的是( )
| A. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| B. | 沸点:CH4>SiH4>GeH4>SnH4 | |
| C. | 熔点由高到低:Al>Mg>Na | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
19.醇广泛存在于自然界中,是一类重要的有机化合物,请判断下列物质中不属于醇类的是( )
| A. | 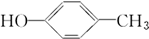 | B. | 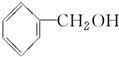 | C. | CH3OH | D. | 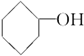 |
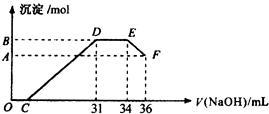 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低(如生成NO、N2O、N2、NH4+等).现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.则
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低(如生成NO、N2O、N2、NH4+等).现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.则