16.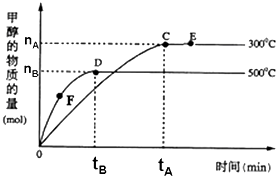 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),根据题意,以下说法正确的是( )
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),根据题意,以下说法正确的是( )
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),根据题意,以下说法正确的是( )
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),根据题意,以下说法正确的是( )| A. | 正反应的△H<0 | |
| B. | 容器中气体的总物质的量E点大于D点 | |
| C. | F点的正反应速率大于逆反应速率 | |
| D. | v(甲醇)=$\frac{{n}_{B}}{3{t}_{B}}$mol/(L•min)表示500℃时反应在D点的速率 |
15. 氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )
氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )
 氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )
氯原子对O3分解有催化作用:Cl+O3=ClO+O2△H1;ClO+O=Cl+O2△H2.大气臭氧层的分解反应是:O+O3=2O2△H,该反应的能量变化示意图如图:下列叙述中,正确的是( )| A. | 反应O+O3=2O2的△H=E1-E3 | B. | O+O3=2O2是放热反应 | ||
| C. | △H=△H1+△H2 | D. | 反应O+O3=2O2的△H=E1-E2 |
14.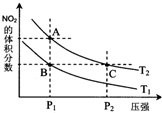 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | A、C两点的反应速率:A>C | |
| B. | A、B两点气体的颜色:A浅,B深 | |
| C. | A、C两点气体的平均相对分子质量:A>C | |
| D. | 由状态B到状态A,可以用加热的方法 |
13.对于冶炼像钠、钙、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法.下列有关说法中正确的是( )
| A. | 目前工业上常用电解熔融氯化钠法制钠,电解时可用铁作阳极 | |
| B. | 电解熔融CaCl2时,金属钙在阳极生成 | |
| C. | 可用电解饱和MgCl2溶液的方法获得金属镁 | |
| D. | 电解熔融Al2O3制备金属铝时,要加入冰晶石,使Al2O3在较低温度下熔解 |
11.下列过程或现象与盐类水解无关的是( )
| A. | 加热蒸干并灼烧FeCl3溶液,得到Fe2O3固体 | |
| B. | 铁在潮湿的环境下生锈 | |
| C. | 明矾净水 | |
| D. | 浓硫化钠溶液有臭味 |
10.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.5 kJ•mol-1,则其燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.5 kJ•mol-1 | |
| B. | 已知2C(石墨,s)+O2(g)=2CO(g);△H=-221 kJ•mol-1,则石墨的燃烧热为110,5 kJ•mol-1 | |
| C. | 已知N2(g)+3H2(g)?2 NH3(g)△H=-92.4 kJ•mol-1,由于△H<0,故该反应一定能自发进行 | |
| D. | 热化学方程式中的化学计量数表示物质的量,可以是分数 |
8.化学与科学、技术、社会、环境密切相关.下列说法正确的是( )
| A. | 盐酸与氢氧化钠的反应可自发进行,因此可用作原电池反应原理 | |
| B. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| C. | 生石灰、铁粉、硅胶是食品包装中常用的干燥剂 | |
| D. | 铝表面可生成一层致密的氧化物薄膜,因此可用铝容器盛装稀硫酸 |
7.下列叙述正确的是( )
0 168967 168975 168981 168985 168991 168993 168997 169003 169005 169011 169017 169021 169023 169027 169033 169035 169041 169045 169047 169051 169053 169057 169059 169061 169062 169063 169065 169066 169067 169069 169071 169075 169077 169081 169083 169087 169093 169095 169101 169105 169107 169111 169117 169123 169125 169131 169135 169137 169143 169147 169153 169161 203614
| A. | 所有的非金属元素都分布在p区 | |
| B. | 在CaO和SiO2晶体中都不存在单个小分子 | |
| C. | 单质中一定含有非极性键 | |
| D. | C2H6是碳链为直线型的非极性分子,可推测C3H4也是碳链为直线型的非极性分子 |

 对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1:
对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1: .(不用注明条件)
.(不用注明条件) .(不用注明条件)
.(不用注明条件) .
.